内钙拮抗剂TMB-8对白皮松花粉管细胞壁构建的影响
【类型】期刊
【作者】白秀峰,刘欣欣,吴小琴,张奠湘(中国科学院华南植物园中国科学院植物资源保护与可持续利用重点实验室;中国科学院研究生院;中国科学院植物研究所中国科学院系统与进化植物学国家重点实验室)
【作者单位】中国科学院华南植物园中国科学院植物资源保护与可持续利用重点实验室;中国科学院研究生院;中国科学院植物研究所中国科学院系统与进化植物学国家重点实验室
【刊名】热带亚热带植物学报
【关键词】 白皮松;花粉管;Ca2+;细胞壁;TMB-8
【资助项】国家自然科学基金项目 (31070161);中国科学院生命科学领域基础前沿研究专项基金 (KSCX2-EW-J-28);中国科学院系统与进化植物学国家重点实验室开放课题基金资助
【ISSN号】1005-3395
【页码】P463-470
【年份】2019
【期号】第5期
【期刊卷】1;|7;|8;|4
【摘要】应用荧光显微技术、激光共聚焦扫描显微技术、单克隆抗体免疫荧光标记技术以及傅里叶变换显微红外光谱分析(FTIR)等手段,研究了内钙拮抗剂TMB-8对白皮松花粉管胞内Ca2+分布、花粉管生长以及细胞壁构建等的影响。结果表明,白皮松花粉管经TMB-8处理后,胞内的Ca2+浓度下降,花粉管内典型的Ca2+浓度梯度消失,花粉萌发和花粉管生长均受到不同程度的抑制,抑制效果与拮抗剂浓度呈正相关。在对照中,纤维素和胼胝质在花粉管细胞壁上均匀分布,酸性果胶质仅分布在花粉管管壁上,而酯化果胶质仅分布于花粉管顶端;经TMB-8处理后,花粉管顶端纤维素、胼胝质以及酸性果胶质含量增加,而酯化果胶质含量减少。这些表明胞内Ca2+对花粉管顶端Ca2+浓度梯度的建成具有重要的作用,抑制胞内Ca2+释放可以影响花粉管细胞壁的结构组成和物理性质,从而抑制花粉管的生长。
【全文】 文献传递
内钙拮抗剂TMB-8对白皮松花粉管细胞壁构建的影响
摘要:应用荧光显微技术、激光共聚焦扫描显微技术、单克隆抗体免疫荧光标记技术以及傅里叶变换显微红外光谱分析(FTIR)等手段,研究了内钙拮抗剂TMB-8对白皮松花粉管胞内Ca2+分布、花粉管生长以及细胞壁构建等的影响。结果表明,白皮松花粉管经TMB-8处理后,胞内的Ca2+浓度下降,花粉管内典型的Ca2+浓度梯度消失,花粉萌发和花粉管生长均受到不同程度的抑制,抑制效果与拮抗剂浓度呈正相关。在对照中,纤维素和胼胝质在花粉管细胞壁上均匀分布,酸性果胶质仅分布在花粉管管壁上,而酯化果胶质仅分布于花粉管顶端;经TMB-8处理后,花粉管顶端纤维素、胼胝质以及酸性果胶质含量增加,而酯化果胶质含量减少。这些表明胞内Ca2+对花粉管顶端Ca2+浓度梯度的建成具有重要的作用,抑制胞内Ca2+释放可以影响花粉管细胞壁的结构组成和物理性质,从而抑制花粉管的生长。
关键词:白皮松; 花粉管; Ca2+; 细胞壁; TMB-8
花粉管是种子植物受精过程中雄性生殖单位的载体,具有典型的顶端极性生长的特点,是近年来研究植物细胞相互识别、胞内和胞外信号传导的模式系统。花粉细胞包被在细胞壁中,花粉管的极性生长依赖于细胞骨架和囊泡的定向运动,不断地将花粉管细胞壁前体物质运送到花粉管顶端合成新壁[1]。花粉管细胞壁除了需要有足够的坚硬性以抵挡内部的膨压,而且也需要一定的柔韧性使得细胞能够不断地伸长[2]。Ca2+是参与调节花粉管生长的重要的信号分子,可以通过钙-钙调素信号通路影响花粉管细胞壁的重塑[1,3]。
花粉管破裂往往发生在顶端,所以通常认为花粉管顶端是最薄弱的地方。为了维持花粉管圆柱形状,花粉管伸长必须有一定的模式,而这种模式恰恰是由从顶端到基部细胞壁的可塑性变化控制的[4]。用免疫荧光化学法、电镜技术等方法对花粉管细胞壁的化学成分进行研究,结果表明,花粉管细胞壁主要含有纤维素、半纤维素、果胶质以及胼胝质等多糖类物质以及细胞壁蛋白。但是不同植物的花粉管,其细胞多糖的组成有所不同,而且不同的培养条件也会影响各种多糖的比例[2,5]。在伸长的花粉管中,纤维素位于花粉管壁的最外层,微纤丝的密度及排列方向可以影响花粉管生长速度[6]。此外,花粉管内合成的果胶多糖,在分泌到囊泡前或在囊泡内会发生甲酯化,甲酯化果胶通过囊泡运输,掺入到花粉管顶端细胞壁[7]。花粉管壁中还含有阿拉伯半乳糖蛋白(arabinogalactan-proteins,AGPs),而且有可能与Ca2+共同参与花粉管壁物质的组装和花粉管的伸长[8]。
运用各种定性或定量的方法现已确证Ca2+在花粉管中呈不均匀分布,Ca2+主要集中在花粉管生长的顶端。花粉管顶端存在浓度极高的Ca2+,且Ca2+浓度呈梯度分布,是所有花粉管生长的一种基本现象,在维持花粉管的各种细胞学事件中起着重要的作用[9]。用胞外Ca2+拮抗剂抑制Ca2+内流,会影响胞内Ca2+浓度梯度的建成以及花粉管的正常生长[10]。然而,有关胞内钙库对花粉管生长影响的研究报道较少[11]。裸子植物的花粉生长与被子植物的相比,具有萌发明间长、生长缓慢等特点,而且二者细胞壁结构与胞内细胞器的组织形式也有较大的差异[11]。因此,Ca2+在被子植物花粉萌发和花粉管生长中的作用机制是否也适用于裸子植物需要进一步的研究。本文利用胞内Ca2+拮抗剂TMB-8 (benzoic acid derivative 3,4,5-trimeth-oxybenzoic acid 8-diethylamino-octyl ester),对胞内Ca2+释放与Ca2+浓度梯度建成、花粉管细胞壁的构建以及裸子植物花粉管生长之间的关系进行研究,为揭示Ca2+在花粉管生长过程中的作用提供科学依据。
1 材料和方法
1.1 供试材料及主要试剂
白皮松(Pinus bungeana Zucc. ex Endl.)花粉采自中国科学院植物研究所。收集白皮松散粉之前的成熟小孢子叶球,置室温下干燥48 h,用无菌干燥小瓶收集成熟花粉,-20℃下密封保存备用。
TMB-8及Calcofluor购自Sigma公司;单克隆抗体JIM5、JIM7 和JIM13购自英国利兹大学Paul Knox实验室。
1.2 花粉培养
称取白皮松花粉10 mg,在室温下平衡30 min,悬浮于10 mL标准液体培养液(15%蔗糖+0.01% H3BO3+0.01% CaCl2),在25℃下摇床(100 r min-1)暗中培养。TMB-8用无水二甲基亚砜溶解,配成10-3 mol/L的贮存液,终浓度梯度设置为0、1、10、25、50及100 μmol/L。按Wu等[10]的方法统计花粉萌发率及花粉管生长速率,当花粉管的长度大于花粉粒的直径时,则认为花粉粒萌发。花粉体外培养36 h后,每隔12 h取少量样品,用4%多聚甲醛固定30 min。在显微镜(OLYMPUS, BX41)下选取已萌发的花粉,用Image-Pro Express 5.1软件(Media Cybernetics, Inc.)测量花粉管基部至花粉管最顶端的长度,每个样品至少测200个花粉管,用t检验分析处理与对照间的差异显著性程度。
1.3 Fluo-3AM低温装载
为了检测生长的花粉管中Ca2+分布状态,选取处于较快生长时期,即培养60 h的花粉管进行荧光标记。在添加不同浓度TMB-8下培养白皮松花粉管60 h后,在培养基中加入1 mmol/L Fluo-3AM至终浓度为10 μmol/L,混匀后于4℃下轻微振荡2 h后取出,室温静置1 h后,在激光扫描共聚焦显微镜(ZEISS LSM 510 META,激发波长488 nm,发射波长522 nm)下对花粉管进行扫描,记录花粉管胞质中Ca2+的分布情况[12]。
1.4花粉管细胞壁的荧光标记
为了检测胞内钙库Ca2+释放受抑制后花粉管细胞壁组成结构的变化,选取白皮松花粉管细胞壁构建已基本稳定的时期,即培养84 h后花粉管生长开始缓慢的时期进行荧光标记。收集并用4%多聚甲醛固定不同浓度TMB-8处理的白皮松花粉管,分别用100 mmol/L的Calcofluor(标记纤维素)以及0.1%水溶性苯胺兰(标记胼胝质)对花粉管细胞壁进行染色,用荧光显微镜(OLYMPUS, BX41)观察拍照[13]。用单克隆抗体JIM5(标记酸性果胶质)、JIM7(标记酯化果胶质)和JIM13(标记AGPs)对花粉管细胞进行孵育[13],用激光扫描共聚焦显微镜(ZEISS LSM 510 META,激发波长488 nm,发射波长522 nm)观察并采集图像。
1.5 傅里叶变换显微红外光谱
用傅里叶变换显微红外光谱(NICOLET MAGNA 750)对正常以及100 μmol/L TMB-8处理后生长84 h的白皮松花粉管顶端细胞壁进行扫描分析,光谱分辨率为8 cm-1,测量范围2000~800 cm-1,扫描次数为128次[14]。
2 结果和分析
2.1 TMB-8对白皮松花粉萌发和花粉管生长的影响
培养84 h后统计花粉萌发率。结果表明,白皮松花粉在标准培养基上培养,萌发率为85.5%,用1 μmol/L和10 μmol/L的TMB-8处理后,花粉萌发率的变化不显著,而25 μmol/L、50 μmol/L和100 μmol/L的TMB-8处理后的花粉萌发率分别为68.5%、57.3%以及38.2%(图1), 经t检验,差异显著或极显著(t25=4.72, P<0.01;t50=7.13, t100=12.28,P<0.001)。对照培养基中的白皮松花粉管的平均生长速率为45.6 μm d-1,花粉管生长正常,长度较长,直径均匀,培养84 h后的花粉管生长缓慢(图2, 图3A)。1 μmol/L和10 μmol/L TMB-8处理后的花粉管生长速率与对照间的差异不显著,分别为45.3 μm d-1和41.6 μm d-1。25 μmol/L、50 μmol/L和100 μmol/L的TMB-8处理后,花粉管长度明显短于对照。花粉管除了生长受到抑制外,形态也发生异常,主要表现为顶端发生膨大(图3:B~D),少量的花粉管有双极性生长现象(图3C)。经25 μmol/L、50 μmol/L和100 μmol/L的TMB-8处理后,花粉管的平均生长速率分别为36.7 μm d-1(t=4.33, P<0.01)、29.5 μm d-1(t=7.84,P<0.001)和23.1 μm d-1(t=10.83, P<0.001),与对照的差异显著或极显著(图2, 图3:B~D)。
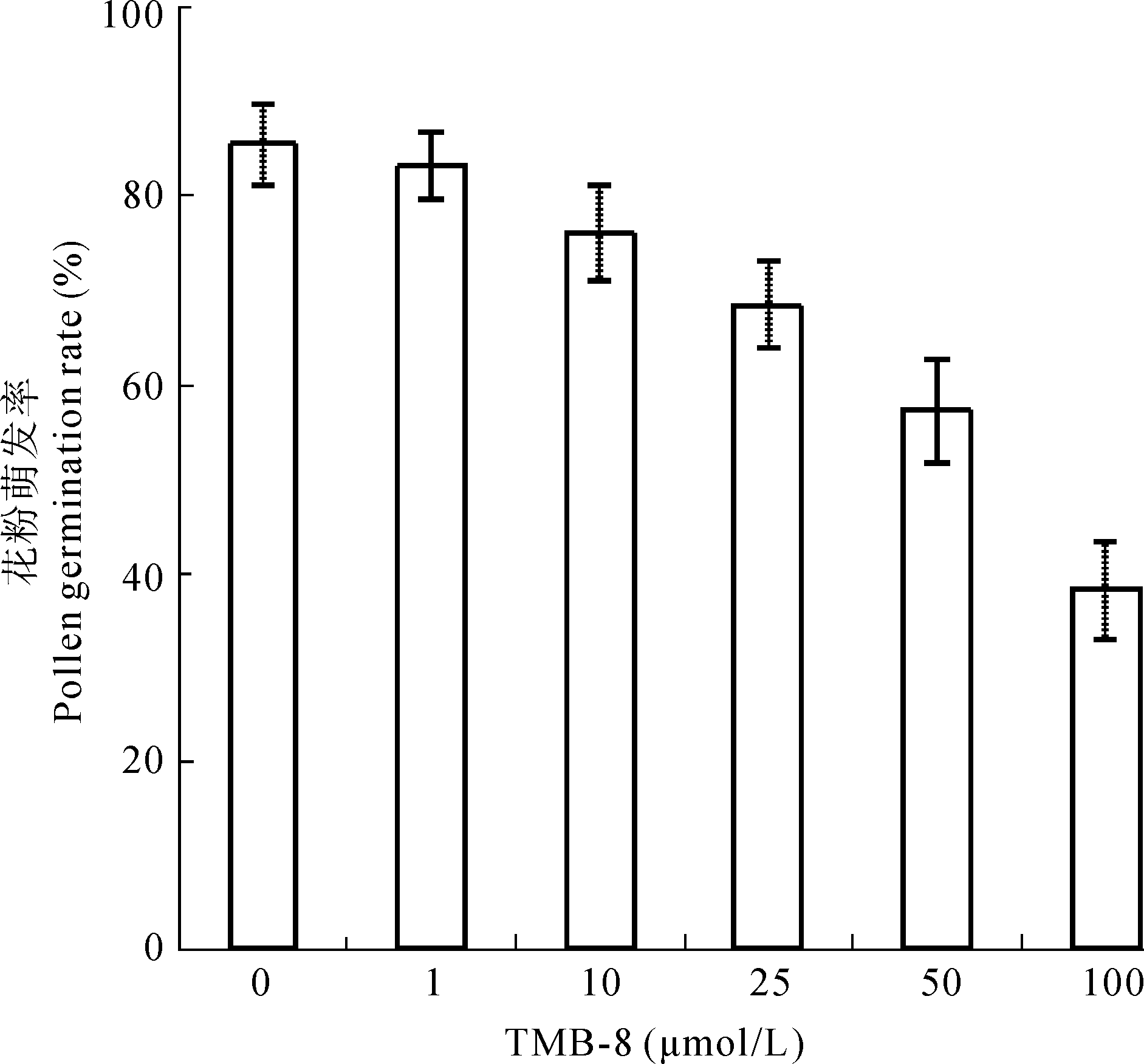
图1 TMB-8对白皮松花粉萌发的影响
Fig. 1 Effect of TMB-8 on pollen germination of P. bungeana
2.2 TMB-8对花粉管中Ca2+分布的影响
通过低温装载将Fluo-3AM探针导入花粉管,从图4可见,正常花粉培养60 h后,花粉管顶端有较强的荧光,而花粉粒和其它部位的荧光较弱,即在生长的花粉管顶端存在明显的Ca2+浓度梯度。而经25 μmol/L、50 μmol/L和100 μmol/L的TMB-8处理后,花粉管中荧光减弱,胞内典型的Ca2+浓度梯度消失(图4)。
2.3 TMB-8对白皮花粉管细胞壁组成构建的影响
正常白皮松花粉管经Calcofluor染色,在整个花粉管壁上均可见荧光分布,而且荧光强度从基部到顶端都较均一(图5A)。用50 μmol/L和100 μmol/L TMB-8处理后,花粉管壁上的纤维素分布与对照相似,但荧光强度不均一,特别是在花粉管膨大的基部以及花粉管最顶端荧光较强(图5:B,C)。用苯胺兰检测花粉管壁中胼胝质的分布情况,结果表明标准培养基上的花粉管壁上的荧光均一分布,花粉萌发孔两侧荧光较强(图5A)。用50 μmol/L TMB-8处理后,花粉管呈波浪状,顶端膨大,花粉管顶端与亚顶端的荧光较对照增强(图5B)。用100 μmol/L TMB-8处理的花粉管侧壁检测不到荧光,而顶端出现了非常强的荧光,说明胼胝质主要沉积在花粉管顶端,而两侧胼胝质含量较低或缺少(图5C)。
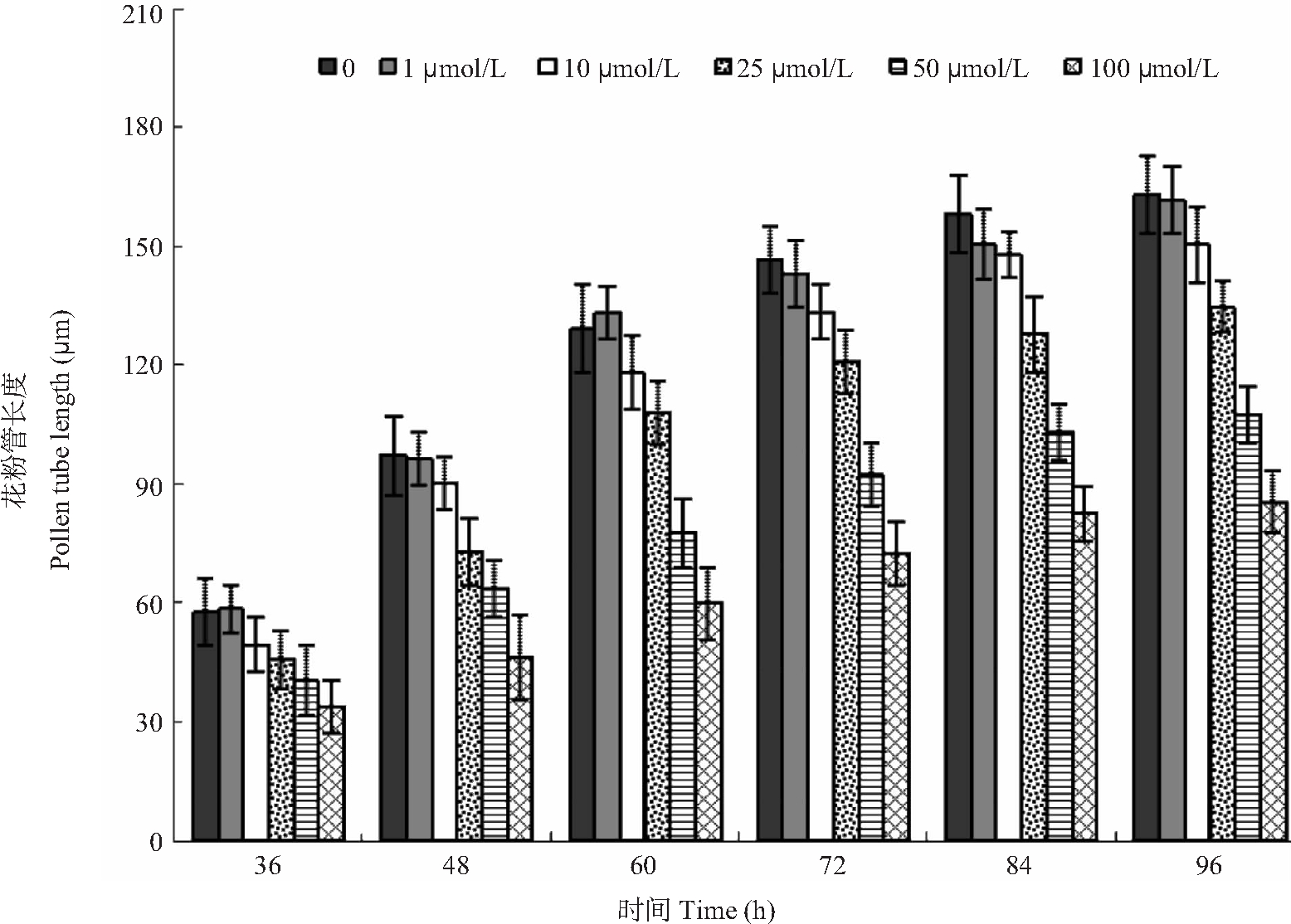
图2 TMB-8对白皮松花粉管生长的影响
Fig. 2 Effect of TMB-8 on pollen tube growth of P. bungeana
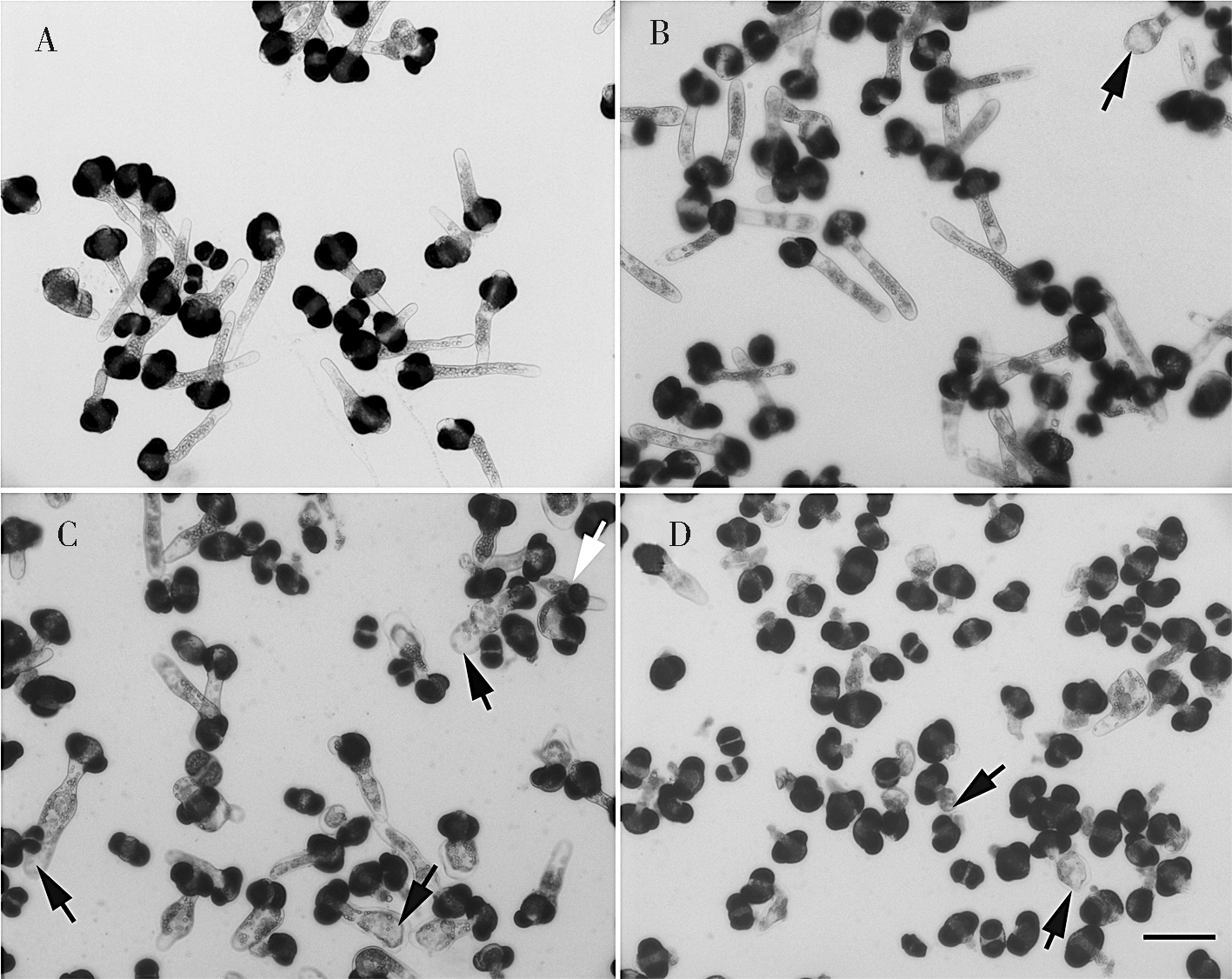
图3 TMB-8对白皮松花粉形态的影响。A. 对照;B. 25 μmol/L TMB-8,偶见花粉管顶端膨大(黑色箭头示);C. 50 μmol/L TMB-8,多数花粉管顶端膨大(黑色箭头示),偶见双极性生长的花粉管(白色箭头示);D. 100 μmol/L TMB-8,萌发的花粉管很短,且多数顶端膨大(黑色箭头示)。Bar=100 μm
Fig. 3 Effects of TMB-8 on pollen tube morphology of P. bungeana. A. Control;B. Few of pollen tube tip swollen (black arrow) cultured with 25 μmol/L TMB-8;C. Most of pollen tube tip swollen (black arrows), and few bipolar growth (white arrow) cultured with 50 μmol/L TMB-8;D. Germinated pollen tubes are short, and most of tip swollen (black arrows) cultured with 100 μmol/L TMB-8. Bar=100 μm
JIM5是识别酸性果胶质的单克隆抗体。花粉管经JIM5孵育后,对照花粉管显示绿色荧光主要分布在花粉管侧壁,而顶端没有检测到荧光(图6A),说明酸性果胶质含量在正常生长的花粉管顶端较低,向花粉管两侧和基部逐渐增加。用50 μmol/L和100 μmol/L TMB-8处理后,顶端出现较强的荧光,花粉管壁两侧的荧光分布与对照相似(图6:B,C)。JIM7是识别酯化果胶质的单克隆抗体。花粉管经JIM7孵育后,对照花粉管显示绿色荧光主要分布在花粉管最顶端的壁上,向花粉管两侧急剧减弱,同时在靠近萌发孔的基部也有荧光分布(图6D)。用50 μmol/L和100 μmol/L TMB-8处理花粉管后,仅在靠近萌发孔的基部检测到荧光(图6:E,F)。JIM13是识别阿拉伯半乳糖蛋白单克隆抗体。花粉管经JIM13孵育后,对照和经50 μmol/L和100 μmol/L TMB-8处理的花粉管,其荧光分布没有发生明显变化,即在整个花粉管壁上都有荧光分布(图6:G~I)。
2.4 花粉管顶端细胞壁的傅里叶变换显微红外光谱分析
比较正常生长84 h和用100 μmol/L TMB-8处理的花粉管顶端细胞壁的红外光谱图,结果表明,TMB-8处理后的花粉管顶端细胞壁组成发生了明显的变化(图7)。在正常培养的花粉管中,饱和酯的特征吸收峰为1740 cm-1,羧酸的特征吸收峰为1589 cm-1和1442 cm-1,蛋白质酰胺的特征吸收峰为1542 cm-1,碳水化合物的吸收峰为1200~900 cm-1;而100 μmol/L TMB-8处理后,花粉管中相应的细胞壁成分的吸收峰强度发生改变。对TMB-8处理的花粉管和对照的图谱进行差谱分析,结果表明,饱和酯特征吸收峰1740 cm-1显示为负值,说明酯化果胶质含量下降;而羧酯特征吸收峰1600 cm-1、1396 cm-1显示为正值,说明酸性果胶质含量经TMB-8处理后含量增加,这与免疫荧光标记的结果一致。同时,碳水化合物(吸收峰分别为1118 cm-1、1056 cm-1和995 cm-1)的含量也显著上升。
3 结论
花粉管的极性生长调控机制是个复杂的过程,涉及钙信号传导、细胞骨架系统参与的囊泡转运以及细胞壁构建等过程[1,15]。在钙信号传导途径中,花粉管顶端Ca2+浓度梯度的建成是首要条件。最近,Wu等[10]利用Ca2+的L型钙通道拮抗剂Nifedipine抑制外源Ca2+内流,首先引起了胞内自由Ca2+浓度的下降、细胞器超微结构异常以及与能量及信号相关的蛋白表达变化,随后进一步导致微丝骨架解聚、胞吞/胞吐的失衡以及细胞壁结构重塑等变化。本研究结果表明,运用胞内Ca2+拮抗剂TMB-8使胞内Ca2+浓度下降,花粉管顶端Ca2+浓度梯度消失,这与最近Chen等[3]对裸子植物白扦(Picea wilsonii)的花粉管生长研究的结果一致,表明了胞内钙库的Ca2+参与了花粉管顶端Ca2+浓度梯度的建成。
花粉管细胞壁的形成及其组成结构直接影响了花粉管的极性生长。花粉管细胞壁的前体物质包括结构蛋白、纤维素、果胶质及胼胝质等多糖类物质。用纤维素合成抑制剂2,6-dichlorobenzonitrile处理,导致花粉管生长受到抑制,顶端膨大[16]。Derksen等[2]认为裸子植物花粉管顶端的纤维素微纤丝密度显著高于被子植物,并据此推测裸子植物花粉管的生长速率明显低于被子植物,可能是因为纤维素含量较高从而限制了花粉管的伸展。而本研究中,白皮松花粉管经TMB-8处理后,其顶端的纤维素荧光增强,这与FTIR光谱图显示的碳水化合物特征峰增强的结果一致,进一步支持了Derksen等[2]有关纤维素含量与花粉管生长关系的推测。
胼胝质的主要成分是β-1,3葡聚糖,其在花粉管壁中的作用还不十分清楚。目前的研究表明,在花粉管生长受抑制时常伴有胼胝质在顶端的累积[3,11]。在Solanum chacoense花粉管中,胼胝质主要分布在花粉管侧壁,而顶端完全没有胼胝质分布[7]。而在正常生长的白皮松花粉管中,胼胝质在顶端及侧壁均有分布,经高浓度胞内Ca2+拮抗剂处理后,胼胝质仅在花粉管顶端累积,表明了胼胝质的合成与分布受钙信号转导网络调控。抑制胞内Ca2+的释放可能通过对胼胝质的代谢调节影响花粉管生长速度。

图4 用Fluo-3AM标记的白皮松花粉管细胞内的Ca2+分布。A: 对照;B: 25 μmol/L; C: 50 μmol/L TMB-8; D: 100 μmol/L TMB-8. Bar=50 μm
Fig. 4 Intracellular Ca2+ distribution in P. bungeana pollen tube marked by Fluo-3AM. A: 对照 Control;B: 25 μmol/L; C: 50 μmol/L TMB-8; D: 100 μmol/L TMB-8. Bar=50 μm
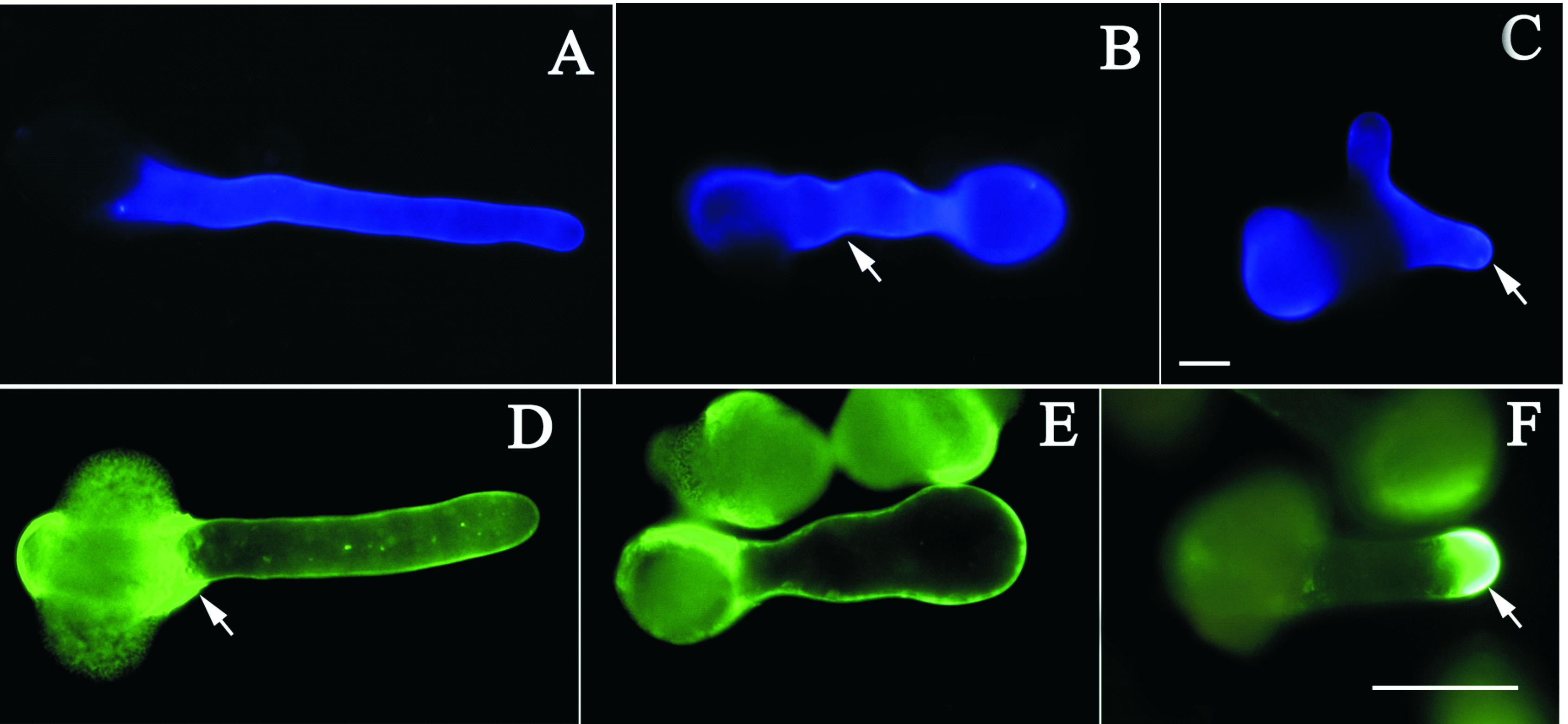
图5 TMB-8对白皮松花粉管细胞壁中纤维素与胼胝质分布的影响。 A~C. 用Calcofluor标记纤维素;A. 对照; B. 50 μmol/L TMB-8; C. 100 μmol/L TMB-8; D~F. 用苯胺兰标记胼胝质;D. 对照; E. 50 μmol/L TMB-8; F. 100 μmol/L TMB-8。白色箭头示花粉管荧光较强区域。A~C. Bar=20 μm; D~F. Bar=50 μm
Fig. 5 Effects of TMB-8 on cellulose and callose distribution in pollen tube cell wall of P. bungeana. A-C. Cellulose marked by Calcofluor;A. Control; B. 50 μmol/L TMB-8; C. 100 μmol/L TMB-8; D-F. Callose marked by aniline blue;D. Control; E. 50 μmol/L TMB-8. F. 100 μmol/L TMB-8. White arrows indicate strong fluorescence regions. A-C. Bar=20 μm; D-F. Bar=50 μm
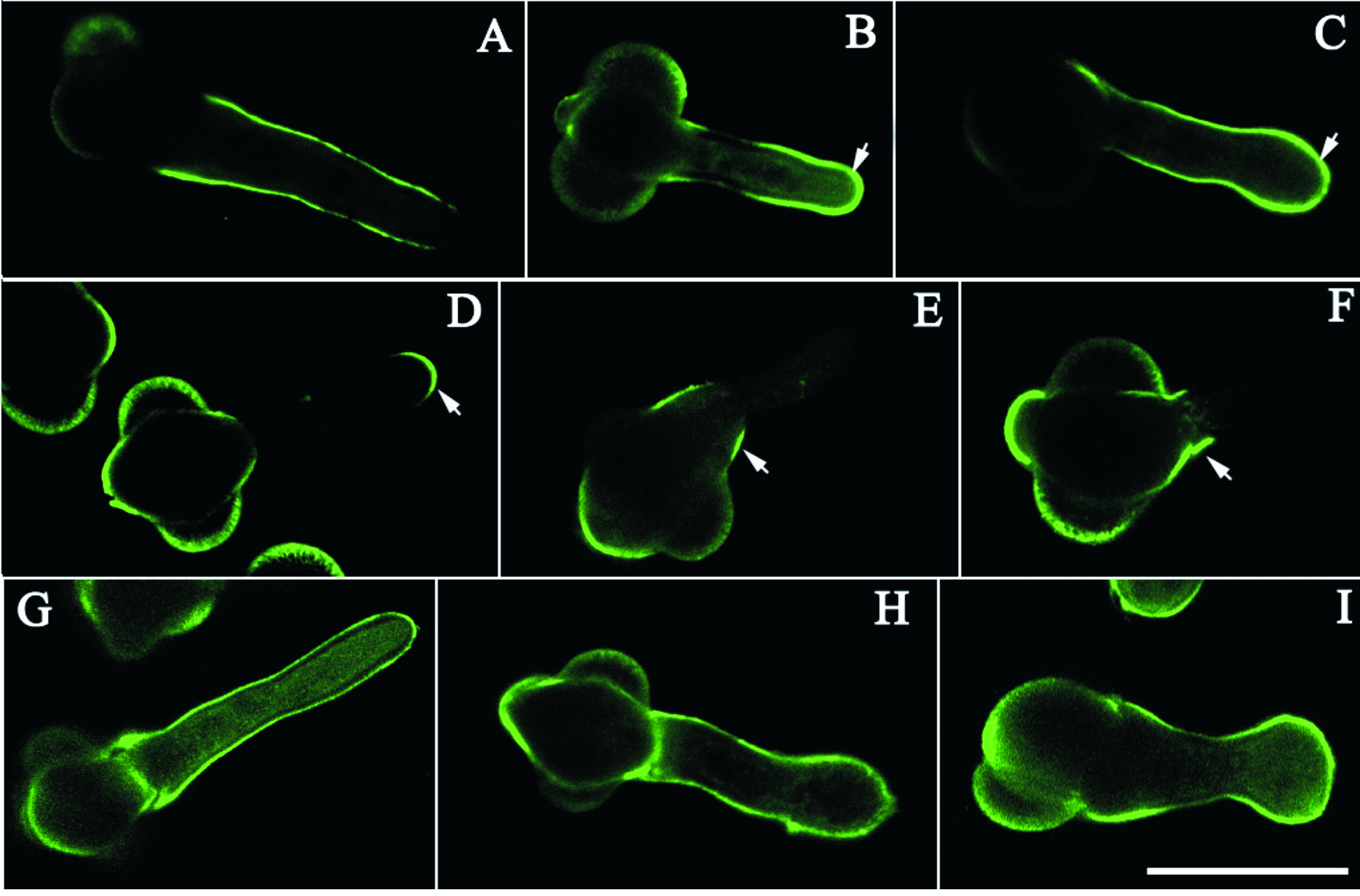
图6 TMB-8对白皮松花粉管细胞壁中果胶质与阿拉伯半乳糖蛋白分布的影响。A~C. JIM5标记酸性果胶质; A: 对照; B: 50 μmol/L TMB-8; C: 100 μmol/L TMB8;D~F. JIM7标记酯化果胶质;D. 对照; E. 50 μmol/L TMB-8; F. 100 μmol/L TMB-8; G~I. JIM13标记阿拉伯半乳糖蛋白;G. 对照; H. 50 μmol/L TMB-8; I. 100 μmol/L TMB-8。箭头示花粉管荧光出现的区域。Bar=40 μm
Fig. 6 Effects of TMB-8 on pectin and AGPs distribution in pollen tube cell wall of P. bungeana. A-C. Acidic pectin marked by JIM5; A: Control; B: 50 μmol/L TMB-8; C: 100 μmol/L TMB8;D-F. Esterified pectin marked by JIM7;D. Control; E. 50 μmol/L TMB-8; F. 100 μmol/L TMB-8; G-I. AGPs marked by JIM13;G. Control; H. 50 μmol/L TMB-8; I. 100 μmol/L TMB-8. Arrows indicate strong fluorescence regions. Bar=40 μm
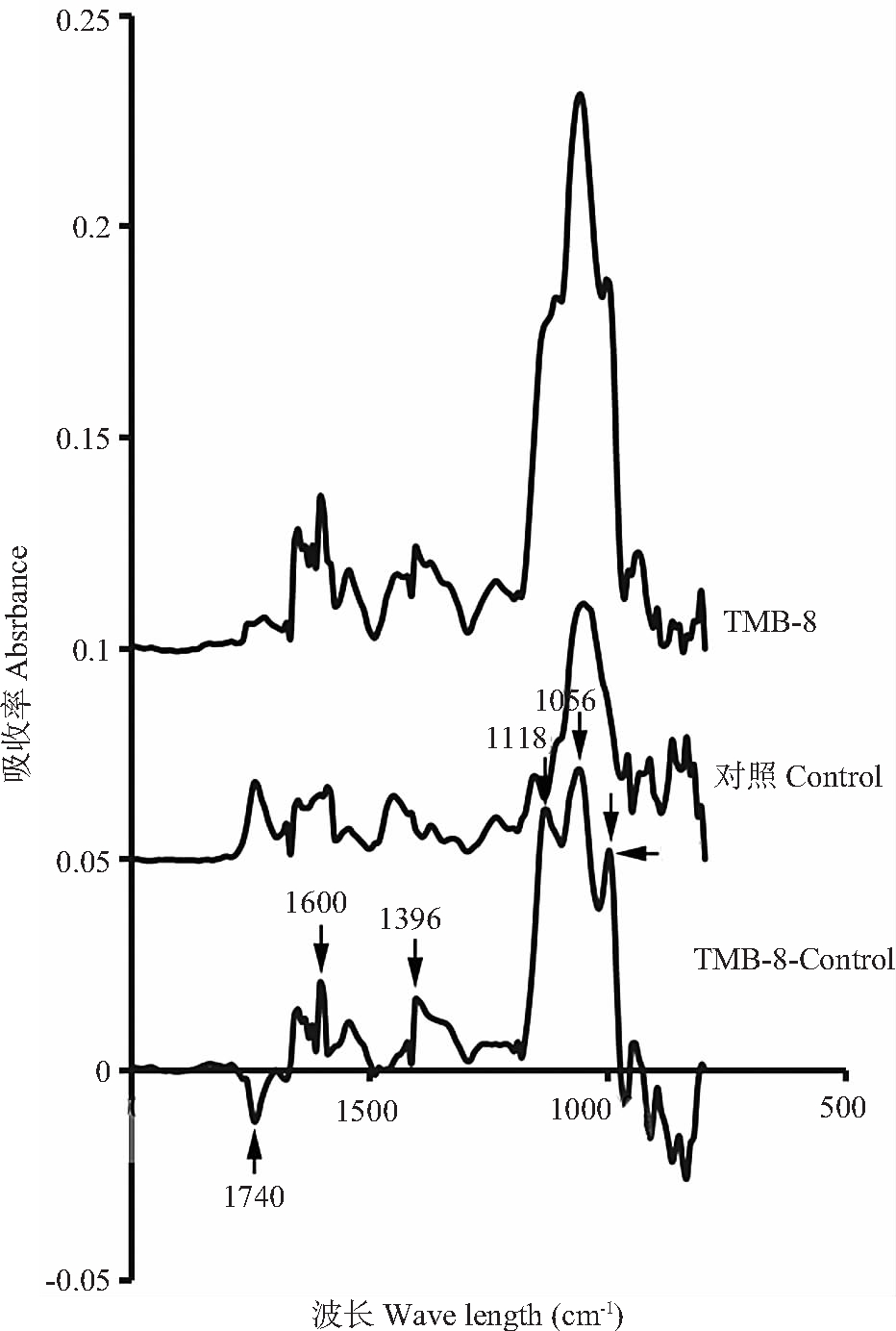
图7 花粉管顶端细胞壁的显微红外光谱和差谱图
Fig. 7 FTIR spectra and FTIR differential spectrum of pollen tube tip cell wall
果胶质是花粉管细胞壁中另一种重要的多糖组成,主要是(1,4)-β-D-半乳聚糖。早期研究结果表明,花粉管细胞的高尔基体中首先合成甲酯化果胶,在质膜上通过依赖于pH和Ca2+果胶甲酯化酶的作用脱酯化形成酸性果胶质,酸性果胶质能与Ca2+以蛋盒结构模式形成交联,以增强细胞壁的机械强度,运用分子生物学手段抑制果胶质甲酯化酶会影响花粉管的正常生长[17-18]。在本研究中,TMB-8处理后花粉管细胞壁中的酸性果胶质与酯化果胶质的分布模式发生显著变化,酸性果胶质在花粉管顶端出现,而酯化果胶质则从花粉管顶端消失。免疫荧光标记的结果与花粉管顶端的FTIR光谱图结果一致。据此我们推测,花粉管经TMB-8处理后,细胞内Ca2+释放通道受抑制,细胞壁钙库的Ca2+无法内流,使得果胶甲酯化酶在高浓度Ca2+下,催化酯化果胶质脱酯化形成酸性果胶的活性增强,从而使酸性果胶质在花粉管顶端含量增加。酸性果胶质通过与Ca2+关联降低了花粉管的延展性,从而使花粉管的生长速率降低。这一结果也支持了Fanklin-Tong提出的胞外钙库与果胶甲酯酶之间存在的正反馈关系[19]。
AGPs不仅是细胞壁蛋白的重要组成之一,而且还通过信号传导途径参与调节花粉管的生长[20-21]。在本研究中,JIM13标记的结果表明,经TMB-8处理的花粉管顶端的AGPs并未有明显变化。而白扦花粉管经TMB-8处理后,其顶端及侧壁中标记的AGPs荧光消失[11],与本研究的结果并不一致。由于花粉与柱头间最初相互识别的物质基础是AGPs的糖基部分[21],因此我们推测胞内Ca2+释放可能是APGs调节花粉管生长的下游事件。
综上所述,本文研究结果表明,胞内Ca2+释放参与了花粉管顶端Ca2+浓度梯度的建成,并进一步通过改变花粉管壁纤维素、胼胝质和果胶质的分布模式,控制花粉管壁的物理化学性质以最终调控花粉管生长。
参考文献
[1] Holdway-Clarke T, Hepler P K. Control of pollen tube growth: Role of ion gradients and fluxes [J]. New Phytol, 2003, 159(3): 539-563.
[2] Derksen J, Li Y Q, Knuiman B, et al. The wall of Pinus sylvestris L. pollen tube [J]. Protoplasma, 1999, 208(1/2/3/4): 26-36.
[3] Chen T, Wu X Q, Chen Y M, et al. Combined proteomic and cytological analysis of Ca2+-calmodulin regulation in Picea meyeri pollen tube growth [J]. Plant Physiol, 149(2): 1111-1126.
[4] Geitmann A. How to shape a cylinder: Pollen tube as a model system for the generation of complex cellular geometry [J]. Sex Plant Reprod, 2010, 23(1): 63-71.
[5] Lennon K A, Lord E M. In vivo pollen tube cell of Arabidopsis thaliana: I. Tube cell cytoplasm and wall [J]. Protoplasma, 2000, 214(1/2): 45-56.
[6] Wu J Z, Lin Y, Zhang X L, et al. IAA stimulates pollen tube growth and mediates the modification of its wall composition and structure in Torenia fournieri [J]. J Exp Bot, 2008, 59(9): 2529-2543.
[7] Parre E, Geitmann A. Pectin and the role of the physical properties of the cell wall in pollen tube growth of Solanum chacoense [J]. Planta, 2005, 220(4): 582-592.
[8] Geitmann A, Steer M. The architecture and properties of the pollen tube cell wall [J]. Plant Cell Monogr, 2006, 3: 177-200.
[9] Iwano M, Entani T, Shiba H, et al. Fine-tuning of the cytoplasmic Ca2+ concentration is essential for pollen tube growth [J]. Plant Physiol, 2009, 150(3): 1322-1334.
[10] Wu X Q, Chen T, Zheng M Z, et al. Integrative proteomic and cytological analysis of inhibitory effect of nifedipine on calcium function in conifer pollen tube [J]. J Proteome Res, 2008, 7(10): 4299-4312.
[11] Chen K M, Wu G L, Wang Y H, et al. The block of intracellular calcium release affects the pollen tube development of Picea wilsonii by changing the deposition of cell wall components [J]. Protoplasma, 2008, 233(1/2): 39-49.
[12] Zhang W H, Rengel Z. Determination of intracellular Ca2+ in cells of intact wheat root: Loading of acetoxymethyl ester of Fluo-3 under low temperature [J]. Plant J, 1998, 15(1): 147-151.
[13] Chen T, Teng N J, Wu X Q, et al. Disruption of Actin filaments by latrunculin B affects cell wall construction in Picea meyeri pollen tube by disturbing vesicle trafficking [J]. Plant Cell Physiol, 2007, 48(1): 19-30.
[14] Wang Q L, Lu L D, Wu X Q, et al. Boron influences pollen germination and pollen tube growth in Picea meyeri [J]. Tree Physiol, 2003, 23(5): 345-351.
[15] Cárdenas L, Lovy-Wheeler A, Kunkel J, et al. Pollen tube growth oscillations and intracellular calcium levels are reversibly modulated by actin polymerization [J]. Plant Physiol, 2008, 146(4): 1611-1621.
[16] Anderson J R, William S, Bedinger P. 2,6-Dichlorobenzonitrile: A cellulose biosynthesis inhibitor, affects morphology and structural integrity of Petunia and lily pollen tubes [J]. J Plant Physiol, 2002, 159(1): 61-67.
[17] Bosch M, Cheung A Y, Hepler P K. Pectin methylesterase: A regulator of pollen tube growth [J]. Plant Physiol, 2005, 138(3): 1334-1346.
[18] Tian G W, Chen M H, Zaltsman A, et al. Pollen-specific pectin methylesterase involved in pollen tube growth [J]. Devel Biol, 2006, 294(1): 83-91.
[19] Franklin-Tong V E. Signaling and the modulation of pollen tube growth [J]. Plant Cell, 1999, 11(4): 727-738.
[20] Mollet J C, Kim S, Jauh G Y, et al. Arabinogalactan proteins, pollen tube growth, and the reversible effects of Yariv phenylglycoside [J]. Protoplasma, 2002, 219(12): 89-98.
[21] Coimbra S, Jone B, Pereira L G. Arabinogalactan proteins (AGPs) related to pollen tube guidance into the embryo sac in Arabidopsis [J]. Plant Sign Behav, 2008, 3(7): 455-456.
Effects of Intracellular Calcium Antagonist, TMB-8, on the Construction of Pollen Tube Wall in Pinus bungeana
Abstract: The effects of TMB-8, an intracellular calcium antagonist, on the pollen tube growth and cell wall construction in Pinus bungeana were investigated by means of fluorescence microscopy, laser scanning confocal microscopy, immunofluorescence technique and Fourier transform infra-red (FTIR) microspectroscopy. The results showed that TMB-8 inhibited P. bungeana pollen germination and tube growth in a dose-dependent manner. Normally growing pollen tubes displayed a typical tip-focused cytosolic free Ca2+ concentration gradient, while the Ca2+ concentration gradient dissipated in TMB-8-treated pollen tubes. Cellulose and callose were distributed uniformly in the wall of pollen tubes; acidic pectin was distributed in the tube wall except for the apex while esterified pectin was present only in the apex. In TMB-8-treated tubes, the content of cellulose, acidic pectin and callose increased while esterified pectin decreased in the apex compared with the normal tube wall. It indicated that the intracellular Ca2+ was necessary in the formation of apical cytosolic Ca2+ concentration gradient. Inhibition of intracellular Ca2+ release resulted in the arrest of pollen tube growth by the modification of cell wall composition in P. bungeana pollen tube.
Key words: Pinus bungeana; Pollen tube; Ca2+; Cell wall; TMB-8
中图分类号:Q944.58
文献标识码:A
文章编号:1005-3395(2011)05-0463-08
doi: 10.3969/j.issn.1005-3395.2011.05.011
收稿日期: 2010-12-07 接受日期:2011-03-18
基金项目:国家自然科学基金项目(31070161); 中国科学院生命科学领域基础前沿研究专项基金(KSCX2-EW-J-28); 中国科学院系统与进化植物学国家重点实验室开放课题基金资助

