五针白皮松组培快繁技术研究*
【类型】期刊
【作者】阮桢媛,乔璐,苏腾伟,白冰,曹玉婵(云南林业职业技术学院)
【作者单位】云南林业职业技术学院
【刊名】西部林业科学
【关键词】 五针白皮松;组培快繁;增殖;试管苗
【资助项】云南省教育厅科学研究基金项目(2014y569,2014y570,2014y571);云南林业职业技术学院科研基金项目[ky(bs)201402,ky(bs)201403]
【ISSN号】1672-8246
【页码】P44-49
【年份】2019
【期号】第4期
【期刊卷】7
【摘要】运用组培快繁技术对极度濒危植物五针白皮松进行大规模扩繁,以改善该物种目前仅依靠有性繁殖且无天然更新造成的种群数量少的现状。通过优化外植体消毒方式、培养基的营养元素及生长激素浓度配比,最终获得最佳试管苗增殖培养基为1/3GD+土豆1%+香蕉1%+6-BA 2.0mg/L+NAA 0.1mg/L,用此培养基诱导培养,植株生长旺盛,增殖系数可达7.95;最佳试管苗生根培养基为1/2MS+土豆1%+香蕉1%+6-BA 0.1mg/L+NAA3.0mg/L,用此培养基进行生根诱导培养,植株生根率为87.00%。此苗木快繁技术流程克服了不定芽增殖率低和生根困难的技术性难题,适用于五针白皮松种苗批量化繁育。
【全文】 文献传递
五针白皮松组培快繁技术研究*
摘要:运用组培快繁技术对极度濒危植物五针白皮松进行大规模扩繁,以改善该物种目前仅依靠有性繁殖且无天然更新造成的种群数量少的现状。通过优化外植体消毒方式、培养基的营养元素及生长激素浓度配比,最终获得最佳试管苗增殖培养基为1/3GD+土豆1%+香蕉1%+6-BA 2.0mg/L+NAA 0.1mg/L,用此培养基诱导培养,植株生长旺盛,增殖系数可达7.95;最佳试管苗生根培养基为1/2MS+土豆1%+香蕉1%+6-BA 0.1mg/L+NAA 3.0mg/L,用此培养基进行生根诱导培养,植株生根率为87.00%。此苗木快繁技术流程克服了不定芽增殖率低和生根困难的技术性难题,适用于五针白皮松种苗批量化繁育。
关键词:五针白皮松;组培快繁;增殖;试管苗
五针白皮松(Pinus squamata)是20世纪90年代发现的仅分布于中国云南省巧家县的珍稀树种[1]。五针白皮松是一种古老的树种,其木材结构细腻,纹理比云南松(Pinus yunnanensis)和华山松(Pinus armandii)直,属于有良好运用前景的用材树种[2]。并且其干形通直,树冠塔形,树皮呈银白色,又是良好的园艺观赏树种[3]。然而,天然状态下的五针白皮松现存立木株数极少,野外种群低于稳定存活界限,有灭绝的危险。此树种于1999年被列为国家一级保护植物,2008年被列入云南省极小种群物种,2010年被列入全球100种最濒危物种名录[4]。
针对五针白皮松具有较高的观赏价值和经济价值,而且处于濒临灭绝的状况,利用组织培养快速繁殖技术扩大五针白皮松种群是一种可行的保护方案。然而,根据国内外众多关于松树组织培养方面的研究报道,松树组织培养快速繁殖技术仍然存在不定芽诱导困难、诱导苗增殖率低以及增殖速度慢等技术性难题[5~6]。导致一系列困难存在的一个重要的可能性原因是目前所使用的普通松树组培培养基营养成分和激素水平不能使得特定松树不定芽和植株很好地增殖与生长。所以,培养基的改良、生长激素浓度以及配比的调节是松树组织培养的一个关键的突破口。本研究将对培养基中的生长激素浓度和配比进行调节,并把土豆和香蕉作为一种天然有机基质添加到培养基中,运用富含天然碳源、氮源和其他微量元素的培养基对五针白皮松进行组培快繁,实现规模化繁育。
1 材料与方法
1.1 试验材料
五针白皮松种子采集于云南省昭通市巧家县药山国家自然保护区,采集时间为2015年3月。
1.2 研究方法
1.2.1 改良培养基的配制
研究所使用的基本培养基为Gresshoff Doy(GD)培养基和Murashige Skoog(MS)培养基。改良培养基中添加土豆和香蕉的量都为1%。先将去皮土豆切成小块,用100倍体积蒸馏水煮烂,冷至室温后将成熟香蕉切碎混入其中,用匀浆机将两者充分打碎,最后混入相应的GD或MS基本培养基中。
1.2.2 种子的消毒
五针白皮松种子消毒采用4种方式:A.先用75%酒精消毒1min,无菌水冲洗2次;再用0.1%升汞溶液消毒10min,无菌水冲洗5次。B.用0.1% 升汞溶液消毒10min,无菌水冲洗5次。C.先在75%的酒精中消毒1min,无菌水冲洗2次;再用2%次氯酸钠溶液消毒15min,无菌水冲洗5次。D.用2%次氯酸钠溶液消毒15min,无菌水冲洗5次。处理后的种子用灭菌滤纸吸干水分,备用。每个消毒处理所使用的种子数为30粒,设置3个重复。消毒后种子接种于萌发培养基(1/3 GD+土豆1%+香蕉1%+蔗糖20g/L+琼脂5g/L)上进行萌发试验,萌发获得种苗用于不定芽诱导。
1.2.3 不定芽诱导
萌发后的种苗生长至4~6cm时,将其切割成小段作为不定芽诱导材料接种到含细胞分裂素和生长素的不定芽诱导培养基中(1/3 GD+土豆1%+香蕉1%+蔗糖20g/L+琼脂5g/L+6-BA 0.05~0.5mg/L+NAA 0.1~0.5mg/L)进行诱导条件优化,为减少试验次数,提高试验效率,各试验均采用双因素混合水平正交试验设计,6-BA设置0.05mg/L、0.1mg/L、0.2mg/L、0.3mg/L、0.4mg/L、0.5mg/L共6个浓度梯度,NAA设置0.1mg/L、0.2mg/L、0.3mg/L、0.4mg/L、0.5mg/L 共5个浓度梯度,两者进行不同浓度组合(共30个处理)。每种培养基接种10瓶,每瓶接种5段,设置3个重复。25±1℃条件下培养4-7天。待诱导出不定芽后,28±1℃条件下继续培养,平均光照时长12h/d,光照强度为1 500lux。
1.2.4 增殖培养
当不定芽长至高度为2~4cm时,将其切割分成小段后分别接种于含有不同浓度细胞分裂素和生长素的GD改良培养基(GD+土豆1%+香蕉1%+蔗糖20g/L+琼脂5g/L+6-BA 0.5~2mg/L+NAA 0.05~0.4mg/L)中进行增殖培养,培养基中6-BA设置0.5mg/L、0.75mg/L、1.0mg/L、1.25mg/L、1.5mg/L、2.0mg/L共6个浓度梯度,NAA设置0.05mg/L、0.1mg/L、0.2mg/L、0.4mg/L共4个浓度梯度,两者进行不同浓度组合(共24个处理)。每种培养基接种10瓶,每瓶接种5段,设置3个重复。28±1℃条件下培养20-25天,平均光照时长14h/d,光照强度为3 000lux。
1.2.5 生根诱导
增殖苗生根诱导培养采用NAA和IAA两种生长素,当继代增殖苗处于生长旺盛时期,将其切割分株后接种于1/2MS改良生根诱导培养基中(1/2MS+土豆1%+香蕉1%+蔗糖20g/L+琼脂5g/L+6-BA 0.1mg/L+NAA/IAA 0.5~3mg/L),进行生根诱导培养,两种生长素浓度设置均为0.5mg/L、1.0mg/L、1.5mg/L、2.0mg/L、2.5mg/L、3.0mg/L。每种培养基接种15瓶,每瓶接种4株,设置3个重复。28±1℃条件下培养20-25天,平均光照时长14h/d,光照强度为3 000lux。
1.2.6 生根苗的壮苗培养和炼苗培养
将诱导出根系的增殖苗适当切割分株后接种于MS改良培养基进行壮苗培养(培养基为,1/2MS+土豆1%+香蕉1%+蔗糖20.0g/L+琼脂5.0 g/L+NAA 0.5mg/L)。28±1 ℃条件下培养10-15天,平均光照时长14h/d,光照强度为3 000lux。壮苗培养过程中,待生根苗的根系长得较为发达,植株长得更旺盛时,对其进行炼苗培养。炼苗培养:第一阶段将生根苗连同组培瓶一起放到大棚内培养,培养温度为25~28℃,光照为大棚内非直接照射的自然太阳光,培养时间为7-14天;第二阶段将瓶苗移栽到经过消毒处理的炼苗土壤中,采用与第一阶段相同的条件培养30-50天。
1.3 评价指标和数据分析
测定内容 消毒种子的污染率、种子萌发率、不定芽增殖系数以及增殖苗的生根率。
评价指标 污染率=种子污染数/接种种子总数×100%;萌发率=萌发种子数/接种种子总数×100%;增殖系数=增殖芽苗总数/接种芽苗数;生根率=生根总苗数/接种总苗数×100%。
统计分析 采用SPSS 13.0软件对试验数据进行计算和分析,测定值在P<0.05水平上进行One-Way ANOVA分析。
2 结果与分析
2.1 不同消毒方法处理效果
4种消毒方式的消毒效果和种子成活率见表1。结果表明,4种消毒方式都具有较好的消毒作用。处理A的效果最佳,污染率可控制在14%范围内;其次是处理B,污染率为18.24%;处理C以及处理D效果稍差,污染率分别为25.41%和30.54%。处理A、B和处理C、D之间的污染率差异显著(P<0.05)。经过A、B、C、D 4种不同方式消毒处理之后,五针白皮松种子在不含生长调节剂的MS培养基中的萌发率分别为61.71%、60.75%、67.48%以及69.35%,但是不同处理之间差异不显著(P>0.05)。
表1 不同消毒剂对五针白皮松种子消毒效果的比较
Tab.1 Comparison of the disinfection effect of different disinfectants to the seeds of Pinus squamata

处理消毒剂消毒时间/min污染率/%萌发率/%A酒精+升汞1+1013.87±1.58a61.71±2.53aB升汞1018.24±2.00a60.75±1.85aC酒精+次氯酸钠1+1525.41±2.34b67.48±3.07aD次氯酸钠1530.54±1.60b69.35±2.80a
注:不同小写字母表示差异显著(P<0.05),下同。
2.2 不定芽诱导结果
如图1所示,在设定的6-BA和NAA浓度范围内,不定芽诱导率均在68%以上,最高可达到91%。两者的浓度逐渐升高时,不定芽诱导率表现出升高趋势,NAA浓度在0.10~0.20mg/L范围内时,不同浓度6-BA处理诱导率变化不显著。当NAA的浓度在0.30mg/L时,诱导率随6-BA浓度增加显著增大。但是当二者浓度均达到0.4和0.5mg/L时,虽诱导率较高,但是不同处理之间差异不显著。从生产成本考虑,二者最佳配比浓度为6-BA 0.4mg/L,NAA 0.4mg/L。
2.3 增殖培养
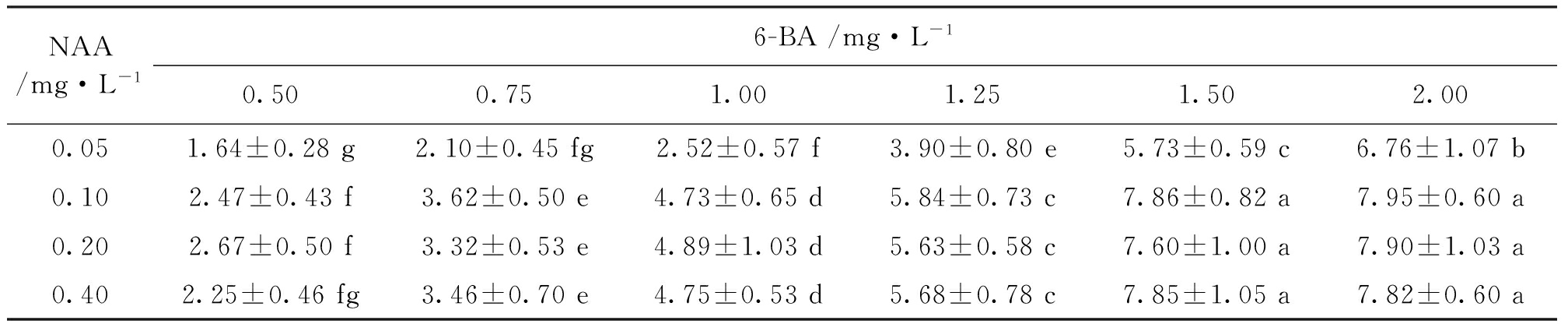
在相对较低浓度生长素(0.05~0.4mg/L NAA)条件下,细胞分裂素(6-BA)对五针白皮松不定芽增殖的影响见表2。由表2可知,无论NAA的浓度高还是低,不定芽的增殖系数没有太大的波动。当6-BA浓度处于最低水平时,NAA处于最低浓度(0.05mg/L)时增殖系数为1.64,NAA处于最高浓度(0.4mg/L)时增殖系数为2.25;当6-BA浓度处于最高水平时,NAA处于最低浓度(0.05mg/L)时增殖系数为6.76,NAA处于最高浓度(0.4mg/L)时增殖系数为7.82。但在6-BA浓度梯度变化范围内,不定芽的增殖系数从1.64升高到7.95。
由此可知,当NAA浓度为0.1mg/L,6-BA浓度在1.5~2.0mg/L范围时增殖效率为7.86~7.95,是五针白皮松不定芽增殖的最佳条件,此条件下五针白皮松不定芽增殖最佳细胞分裂素和生长素浓度比例范围是15︰1~20︰1。
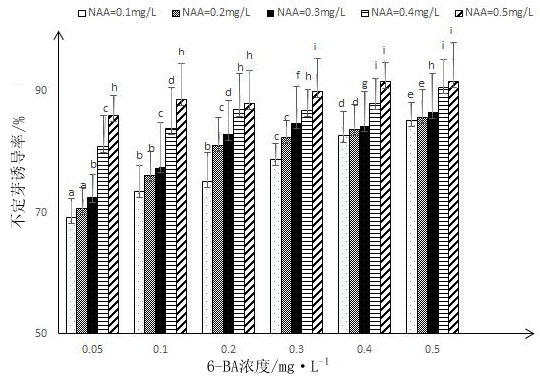
图1 不同浓度6-BA和NAA组合不定芽诱导率
Fig.1 Formation of adventitious buds enhanced by the treatments of the different concentration levels of 6-BA and NAA
表2 不同浓度6-BA和NAA促进五针白皮松试管苗增殖系数
Tab.2 The propagation coefficients of the test-tube plantlet promoted by the different concentrations of 6-BA and NAA
NAA/mg·L-16-BA/mg·L-10.500.751.001.251.502.000.051.64±0.28g2.10±0.45fg2.52±0.57f3.90±0.80e5.73±0.59c6.76±1.07b0.102.47±0.43f3.62±0.50e4.73±0.65d5.84±0.73c7.86±0.82a7.95±0.60a0.202.67±0.50f3.32±0.53e4.89±1.03d5.63±0.58c7.60±1.00a7.90±1.03a0.402.25±0.46fg3.46±0.70e4.75±0.53d5.68±0.78c7.85±1.05a7.82±0.60a
2.4 不同生长素对增殖苗的生根诱导
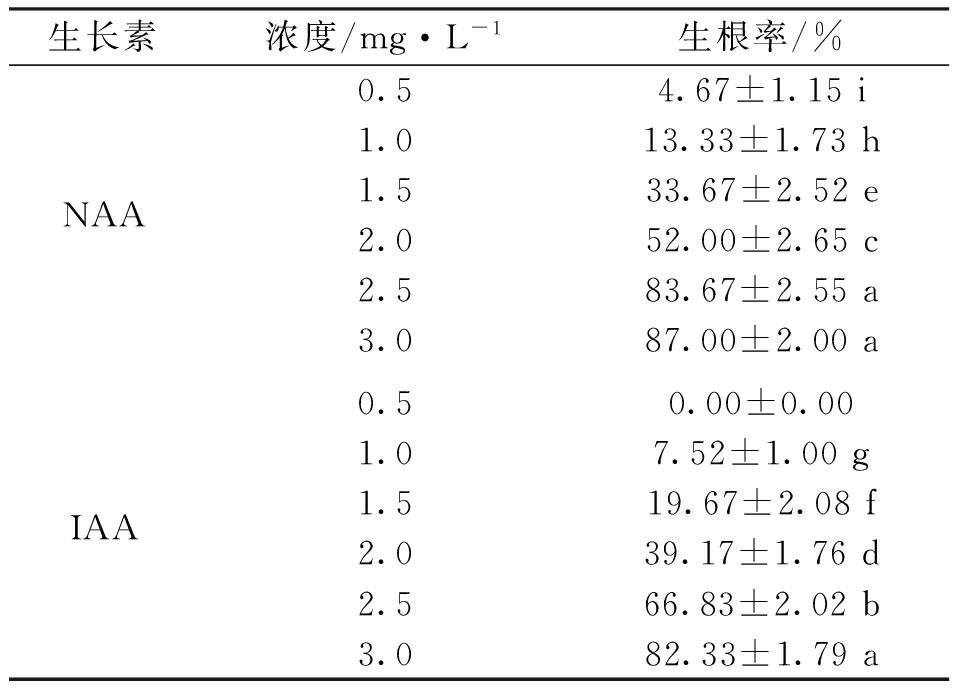
表3显示,生根率随NAA浓度的升高而升高,当NAA浓度为2.5mg/L和3mg/L时,生根率可分别达到83.67%和87%,两者无显著差异,但与其他处理差异显著。
从数据统计结果可以看出,IAA对五针白皮松增殖苗的生根诱导同样起到较好的促进效果。但IAA最佳有效浓度为3mg/L,比NAA的最佳有效浓度3mg/L略低,此条件下的生根率为82.33%。在生长素浓度范围为0.5~2.5mg/L之间时,使用IAA诱导的生根率要显著低于使用NAA诱导的生根率。当IAA浓度低于1.5mg/L时,增殖苗难以诱导生根(表3)。
表3 不同浓度NAA、IAA对五针白皮松试管苗生根诱导的生根率
Tab.3 The percentages of taking root of the test-tube plantlet promoted by the different concentrations of NAA,IAA
生长素浓度/mg·L-1生根率/%NAA0.54.67±1.15i1.013.33±1.73h1.533.67±2.52e2.052.00±2.65c2.583.67±2.55a3.087.00±2.00aIAA0.50.00±0.001.07.52±1.00g1.519.67±2.08f2.039.17±1.76d2.566.83±2.02b3.082.33±1.79a
2.5 壮苗和炼苗培养
为了更有利于生根苗的生长,将已经生根的五针白皮松增殖苗转移到不含细胞分裂素但含有较低浓度NAA(0.5mg/L)的培养基中继续培养,使其根系更发达,植株生长更茂盛。待植株根系长度超过5cm时,将试管苗转移到温室里,使用遮荫网控制光照以弱自然光照培养1周,再采用完全自然光照培养1周。然后将植株移出培养瓶用清水洗净,栽到红土与河沙混合的基质里进行培养。大棚空气湿度控制在80%以上,每天早晨对培养基质进行浇水。2周后不发生死亡的植株在后期移栽过程中都能存活。
3 结论与讨论
五针白皮松组织培养研究中存在诱导芽褐化和玻璃体化等问题,从而导致芽诱导困难、诱导苗增殖率低以及增殖速度慢等现象[6]。针对五针白皮松的生长特性及其快繁存在的难题,本研究对最适合用作松树组培快繁的植物生长素(NAA和IAA)以及细胞分裂素(6-BA)在五针白皮松组培快繁中的使用浓度进行了优化和改进,同时也对培养基的基本元素进行了调整。这些优化调整在很大程度上降低了组培苗的褐化和玻璃体化,明显改进了五针白皮松在快繁过程中的增殖和生根。并且天然基质和营养元素的添加不仅使得组培苗增殖生长更加旺盛,而且还使得其生根成活率更高。此研究中的苗木组织培养快速繁殖技术可以对五针白皮松进行工业化繁殖育苗,以经济高效的方式扩大其优良种源。
五针白皮松种子在自然条件下能够萌发生长,在温度、水分以及其他条件都适当的情况下一般1周能够萌发,但在逆境条件下则需要更长时间,甚至不能萌发[3~4]。采用酒精和0.1%升汞对种子进行连续消毒后,能够将种子无菌萌发的污染率控制在相对较低水平。消毒后60%以上的种子仍然能够萌发和成活。种子的发芽率并非完全受消毒的影响,但消毒时间过长会造成药剂的过量残留无法清洗干净,从而影响种子的萌发。所以酒精消毒的时间设定为较短的1min,升汞和次氯酸钠消毒的时间分别设定为相对较长的10min和15min。
许多植物生长激素对不定芽或是外植体的诱导培养都具有很好的促进作用,这些激素主要包括6-苄基腺嘌呤(6-BA)、2,4-二氯苯氧乙酸(2,4-D)、玉米素、激动素(CK)、萘乙酸(NAA)、吲哚乙酸(IAA)以及赤霉素(GA3)[7]。在本研究中,不定芽的诱导率随着NAA和6-BA浓度的增加而增加,但是当二者浓度均达到0.4mg/L和0.5mg/L时,虽诱导率增加但差异不显著,故在诱导试验时可在获得较高诱导率前提下选用较低水平生长激素浓度。
对于树木愈伤组织、定芽和不定芽的诱导,不同种类的生长素和细胞分裂素配合使用,一般能够有较好的增殖促进效果[8]。特别是相对较高浓度的细胞分裂素6-BA,较低浓度的生长素NAA和IAA,对大多数松树试管苗的增殖有较好的诱导和促进作用[9]。本研究中五针白皮松不定芽的诱导以GD培养基为基础,其中适当地添加土豆和香蕉泥,在细胞分裂素和生长素以及丰富的营养元素的共同作用下,获得的最高不定芽增殖系数为7.95。在NAA浓度为0.05mg/L、0.1mg/L、0.2mg/L以及0.4mg/L条件下,五针白皮松不定芽增殖量随着6-BA浓度水平的升高而增高。当NAA浓度在较低浓度水平时,6-BA浓度达到1.5mg/L时就能够起到很好的促进增殖效果。但是,在组培快繁过程中,过高的细胞分裂素浓度水平容易造成愈伤组织或不定芽的畸形生长和遗传变异[7]。因此,细胞分裂素浓度控制在相对较低的有效水平为宜。
相对较高浓度的生长素能够缩短试管苗嫩梢不定根形成的时间,并促进根的形成[10]。NAA和IAA都具有较好的促进植物生根效果,本研究采用这2种生长素,在0.5~3.0g/L浓度范围进行五针白皮松增殖苗生根诱导培养。由不同浓度条件下NAA和IAA对增殖苗的生根诱导效果可见,相同浓度条件下NAA的促进生根效果优于IAA,当浓度水平在2.5~3.0mg/L范围内时NAA诱导增殖苗的生根率接近90%。所以,选用NAA(2.5mg/L)作为生根诱导剂可以实现对五针白皮松增殖苗的工业化生根诱导培养。
参考文献:
[1]李乡旺.云南松属一新系一新种[J].云南植物研究,1992,14(3):259-260.
[2]王昌命,李乡旺,木乔英,等.五针白皮松(Pinus squamata)的木材构造及其归类研究[J].四川农业大学学报,1998,16(1):165-169.
[3]陆素娟,王泾,朱惠萍.五针白皮松生物学特性的研究[J].西南林学院学报,1999,19(2):86-89.
[4]陆素娟,邓莉兰,李乡旺.五针白皮松濒危原因初步研究[J].西南林学院学报,1999,14(1):42-44.
[5]Gupta P K,Durzan D J.Shoot multiplication from mature trees of Douglas-fir(Pseudotsuga menziesii)and sugar pine(Pinus iambertiana)[J].Plant Cell Reports,1985,4:177-179.
[6]普晓兰,林萍,李乡旺.五针白皮松离体胚培养初步研究[J].西南林学院学报,1997,17(1):17-20.
[7]乔治E F,阿尔M A,克勒克G J.植物组织培养[M].北京:化学工业出版社,2015:171-183.
[8]Noh E W,Minocha S C,Riemenschneide D E.Adventitious shoot formation from embryonic explants of red pine(Pinus resinosa)[J].Physiologia Ppantarum,1988,74(1):119-124.
[9]Vargas-hernandez J J,Gonzalez R H.In vitro morphogenesis of Pinus patula[J].Cham Rvista Chapingo,1992,15(75):7-17.
[10]Mathur G N.In vitro plantlet regeneration from mature zygotic embryos of Pinus wallichiana A.B[J].Jacks.Plant Cell Reports,1999,19(1):74-80.
A Study on Tissue Culture of Pinus squamata
Abstract:The critically endangered Pinus squamata now only reproduced by seed,and no natural regeneration was found.In order to expand its population,the focus of this study was to culture this species in industrial scale by the technology of tissue culture and rapid propagation.The disinfection for explant,the ratios of plant growth hormones and nutrients in culture medium have been optimized.The components of culture medium which is most appropriate for the propagation of test-tube plantlets as follow:1/3 GD+mashed potato 1%+mashed banana 1%+6-BA 2.0mg/L+NAA 0.1mg/L.The growth of plantlets was strong and its propagation coefficient could reach 7.95 when cultured with optimized propagation medium.And the optimized components of medium for test-tube plantlets to taking root as follow:1/2 MS+mashed potato 1%+mashed banana 1%+6-BA 0.1mg/L+NAA 3.0mg/L.The percentage of taking root could reach 87% in this study.The propagation and roots formation of plantlets have been significantly improved by the optimized technology of tissue culture and rapid propagation,and this technology is suitable for the mass seedling breeding of Pinus squamata.
Key words:Pinus squamata;tissue culture;rapid propagation;test-tube plantlets
中图分类号:S 791.24
文献标识码:A
文章编号:1672-8246(2017)04-0044-06
收稿日期:2017-04-10
基金项目:云南省教育厅科学研究基金项目(2014Y569,2014Y570,2014Y571),云南林业职业技术学院科研基金项目〔KY(BS)201402,KY(BS)201403〕。
doi:10.16473/j.cnki.xblykx1972.2017.04.009

