针叶树GID1同源基因分离鉴定与功能预测
【类型】期刊
【作者】张运城,周长虹,钮世辉,李伟(北京林业大学生物科学与技术学院,林木育种国家工程实验室;河北省木兰围场国有林场管理局)
【作者单位】北京林业大学生物科学与技术学院,林木育种国家工程实验室;河北省木兰围场国有林场管理局
【刊名】北京林业大学学报
【关键词】 赤霉素;针叶树;GID1基因;分离鉴定;功能预测
【资助项】国家自然科学基金项目(31370657);“948”国家林业局引进项目(2012-4-40)
【ISSN号】1000-1522
【页码】P40-48
【年份】2019
【期号】第5期
【期刊卷】1;|7;|8;|4;|5;|2
【摘要】GID1作为赤霉素(GA)受体蛋白,是GA信号通路的重要组成部分,其编码基因GID1在被子植物中已经被广泛克隆,但在针叶树种中的研究十分滞后。为了分离针叶树GA受体GID1基因并推测其功能,本研究以拟南芥GID1s序列为探针,在油松高质量参考转录组内筛选并鉴别出了油松GID1直系同源基因;基于该基因序列同源克隆了樟子松、白皮松、赤松GID1基因,通过BLAST获得了日本落叶松、火炬松、白云杉与挪威云杉的GID1-like基因;对针叶树GID1基因进行序列保守性、蛋白结构和组织表达活性分析。结果表明:针叶树种很可能只含有一个GID1基因,该基因在针叶树中具有很高的保守性;虽然与被子植物GID1之间的序列一致性较低,但其保持GA亲和活性所必需的氨基酸残基十分保守,与其下游DELLA蛋白相互作用的功能域与结构同样十分保守,推测其在针叶树GA信号转导中具有受体功能;表达分析显示GID1在挪威云杉不同组织和油松雌雄球花不同发育阶段间表达较为稳定,表明GID1可能广泛参与这些组织的发育过程,针叶树GA信号调控通路中GA受体的转录调控可能并不是核心调控机制。研究结果为GID1基因在针叶树生长发育过程中的分子调控机制研究奠定了基础。
【全文】 文献传递
针叶树GID1同源基因分离鉴定与功能预测
摘要:GID1作为赤霉素(GA)受体蛋白,是GA信号通路的重要组成部分,其编码基因GID1在被子植物中已经被广泛克隆,但在针叶树种中的研究十分滞后。为了分离针叶树GA受体GID1基因并推测其功能,本研究以拟南芥GID1s序列为探针,在油松高质量参考转录组内筛选并鉴别出了油松GID1直系同源基因;基于该基因序列同源克隆了樟子松、白皮松、赤松GID1基因,通过BLAST获得了日本落叶松、火炬松、白云杉与挪威云杉的GID1-like基因;对针叶树GID1基因进行序列保守性、蛋白结构和组织表达活性分析。结果表明:针叶树种很可能只含有一个GID1基因,该基因在针叶树中具有很高的保守性;虽然与被子植物GID1之间的序列一致性较低,但其保持GA亲和活性所必需的氨基酸残基十分保守,与其下游DELLA蛋白相互作用的功能域与结构同样十分保守,推测其在针叶树GA信号转导中具有受体功能;表达分析显示GID1在挪威云杉不同组织和油松雌雄球花不同发育阶段间表达较为稳定,表明GID1可能广泛参与这些组织的发育过程,针叶树GA信号调控通路中GA受体的转录调控可能并不是核心调控机制。研究结果为GID1基因在针叶树生长发育过程中的分子调控机制研究奠定了基础。
关键词:赤霉素;针叶树;GID1基因;分离鉴定;功能预测
赤霉素(Gibberellins,GAs)是一种重要的双萜类植物激素,参与植物生长发育的许多重要过程,包括种子发芽、花芽分化、叶片伸展、木质部发育等[1-5]。从20世纪50年代人们发现外施赤霉素能够明显作用于针叶树球花发育起,国内外育种工作者利用赤霉素对多种针叶树种进行了研究,在促进针叶树开花和诱导雌雄球花分化方面积累了大量的经验[6-7]。松科树种施用GA4、GA7等极性较小的赤霉素,能够明显促进其开花和球果发育。马尾松(Pinusmassoniana)施用GA1/3和GA4/7能促进其雌雄球花发育[8],欧洲赤松(P.sylvestris)球花发育后期施用GA4/7能显著增加雌花[9],38年生西部落叶松(Larixoccidentalis)施用GA4/7可促进其开花[10]。虽然赤霉素在针叶树中已经广泛应用于育种实践工作,但是其作用的分子机制研究却尚未开展。
近年来人们对赤霉素的合成及代谢途径有了深入的认识,其信号转导途径的研究也随着水稻(Oryzasativa)中赤霉素可溶性受体GID1 (Gibberellin insensitive dwarf1)的发掘而有了突破性进展[11-12]。GID1是赤霉素信号转导的关键因子之一,与GA结合后可以介导植物生长抑制因子DELLA蛋白的泛素化降解,产生赤霉素效应,促进植物生长。由于GID1含有激素敏感性脂肪酶(Hormone sensitive lipase,HSL)超基因家族同源的保守序列,因此在植物体内存在许多相似序列,但其中只有极少数成员具有GA结合活性。水稻中目前仅发现了1个[11],而Nakajima等[13]在鉴定拟南芥(Arabidopsisthaliana)赤霉素受体时发现了超过10条和OsGID1基因相似的序列,但部分基因编码的氨基酸序列在和GA结合的关键位点发生了突变,功能验证表明只有3个基因具有GA受体功能,因而推测针叶树中GID1基因可能也很少。同时针叶树基因组庞大,测序成本较高并且与被子植物进化距离较远,这给针叶树GID1直系同源基因的克隆带来了很大困难,因此至今没有任何针叶树GID1基因被系统研究,严重阻碍了针叶树GA作用机制相关研究的进展。
目前针叶树中具有功能的GID1基因尚未确定,而GID1作为赤霉素信号转导途径的关键调控因子之一,对针叶树中赤霉素作用的分子机制研究具有重要意义。为了探究针叶树中GID1同源基因的数量及其是否具有受体功能,本研究以拟南芥GID1s序列为探针对油松转录组进行了比对,通过系统发育分析确定GID1的直系同源基因。而后又对樟子松(P.sylvestrisvar.mongolica)、白皮松(P. bungeana)、赤松(P.densiflora)、火炬松(P.taeda)、白云杉(Piceaglauca)、挪威云杉(P.abies)、日本落叶松(L.kaempferi)GID1同源基因进行克隆与序列分析,并通过系统发育树了解GID1基因的进化地位。对挪威云杉和油松GID1在不同时期和不同组织的表达量进行分析,推测其在针叶树生长发育过程中的作用。研究结果为GID1基因在针叶树生长发育过程中的分子调控机制研究奠定了基础。
1 材料与方法
1.1 植物材料
本研究所用材料:油松、白皮松取自北京林业大学校园,樟子松取自河北围场龙头山种苗场,赤松来自山东省林业科学研究院。
1.2 针叶树GID1同源基因的克隆与鉴定
利用拟南芥与水稻GID1的氨基酸序列: AtGID1a(AT3G05120)、AtGID1b(AT3G63010)、AtGID1c(AT5G27320)和OsGID1(Os05g0407500)与油松参考转录组(NCBI登录号:SRA056887)进行TBLASTN比对,每次比对保留最相似的5条序列,将筛选到的序列剔除重复后再与拟南芥和水稻GID1序列通过最大似然法(Maximum likelihood, ML)构建进化树,获得相似性最高的5条序列。将筛选到的序列与其他针叶树转录组序列(http:// dendrome.ucdavis.edu)和P.taeda基因组(http:// loblolly.ucdavis.edu/bipod/ftp/Genome_Data/ genome/pinerefseq/Pita/v1.01)进行比对,判定这些序列是否为同一基因的不同区域并进行CDS预测。对不包含全长CDS的基因序列设计特异引物,利用特异引物分别与pUC19载体插入位点两端引物对油松全长cDNA文库进行扩增,对上下游扩增片段克隆测序后进行拼接。将获得的油松GID1相似蛋白序列与拟南芥全基因组进行TBLASTN比对,获取拟南芥中与它们相似的蛋白序列,用MUSCLE[14-15]对所得全部基因的全长蛋白序列进行多重比对,基于JTT模型构建ML系统进化树,确定GID1同源基因,Bootstrap值通过1 000次bootstrap重复获得。
根据获得的GID1同源基因设计通用引物, Conifer/GID1-F:atggcttccagcgatgattatggattcaac,Conifer/ GID1-R:gatgaagcatttggctaaagttccggaacc,以樟子松、白皮松、赤松的基因组DNA为模板进行PCR扩增,回收片段经蓝白斑筛选后测序。日本落叶松、火炬松、白云杉与挪威云杉序列信息从针叶树公共数据库(http://dendrome.ucdavis.edu)获得。
1.3 针叶树GID1基因的序列分析
将所得8种针叶树基因的氨基酸序列和江南卷柏(Selaginellamoellendorffii)、小立碗藓(Physcomitrellapatens)以及水稻、拟南芥等已获得功能验证的GID1蛋白的氨基酸序列用ClustalX和GeneDoc进行多重比对,利用MEGA6.0基于JTT模型构建ML系统进化树,Bootstrap值通过1 000次bootstrap重复获得。利用SWISS-MODEL(http:// swissmodel.expasy.org)进行蛋白质3D模型模拟[16]。
GenBank ID:白云杉:P.glaucaGID1 (BN001190.1),日本落叶松:L.kaempferiGID1 (KF515230.1),火炬松:P.taedaGID1 (BN001190.1),小立碗藓:PpGID1L1(XM_ 001757014.1)、PpGID1L2(EU262749.1),江南卷柏:SmGID1a(XM_002978792.1)、SmGID1b(XM_ 002993346.1)。
1.4 针叶树GID1基因表达模式分析
挪威云杉GID1基因(MA_855574g0010)在不同时期及不同组织中的表达量数据从云杉基因组数据库的exPlot中获得(http://congenie.org/explot)。将油松雌雄球花从表型可辨别到发育成熟分为6个阶段,在北京林业大学校园内选定3株成熟油松,每个阶段分别采样并构建测序文库,利用Illumina Hiseq 2000(Illumina,USA)第二代高通量测序平台进行测序,利用Tophat[17-18]计算GID1在每个阶段的表达丰度,基因表达量用RPKM(reads per kilobase permillion reads)表征。
2 结果与分析
2.1针叶树GID1同源基因克隆与鉴定
以拟南芥与水稻GID1的氨基酸序列为探针,在油松参考转录组中进行BLAST,共获得了5个与GID1相似性最高的序列,并进行了全长CDS克隆,分别命名为PtGID1、PtGID1-L1、PtGID1-L2、PtGID1-L3、PtBSU1。但基于BLAST的相似性只能反映序列的相似程度,并不能区分它们的同源关系。为了避免建树时因序列相似度高而筛选到非直系同源基因,又将所得序列与拟南芥全基因组进行比对,反选到20个相似性最高的基因。基于所有基因的氨基酸序列构建ML进化树(图1),结果表明,通过反选获得的基因能够很好地将这5个序列的关系区分开来,只有PtGID1和水稻与拟南芥的GID1聚为一类,属直系同源基因,而其余4个基因与其进化距离较远。
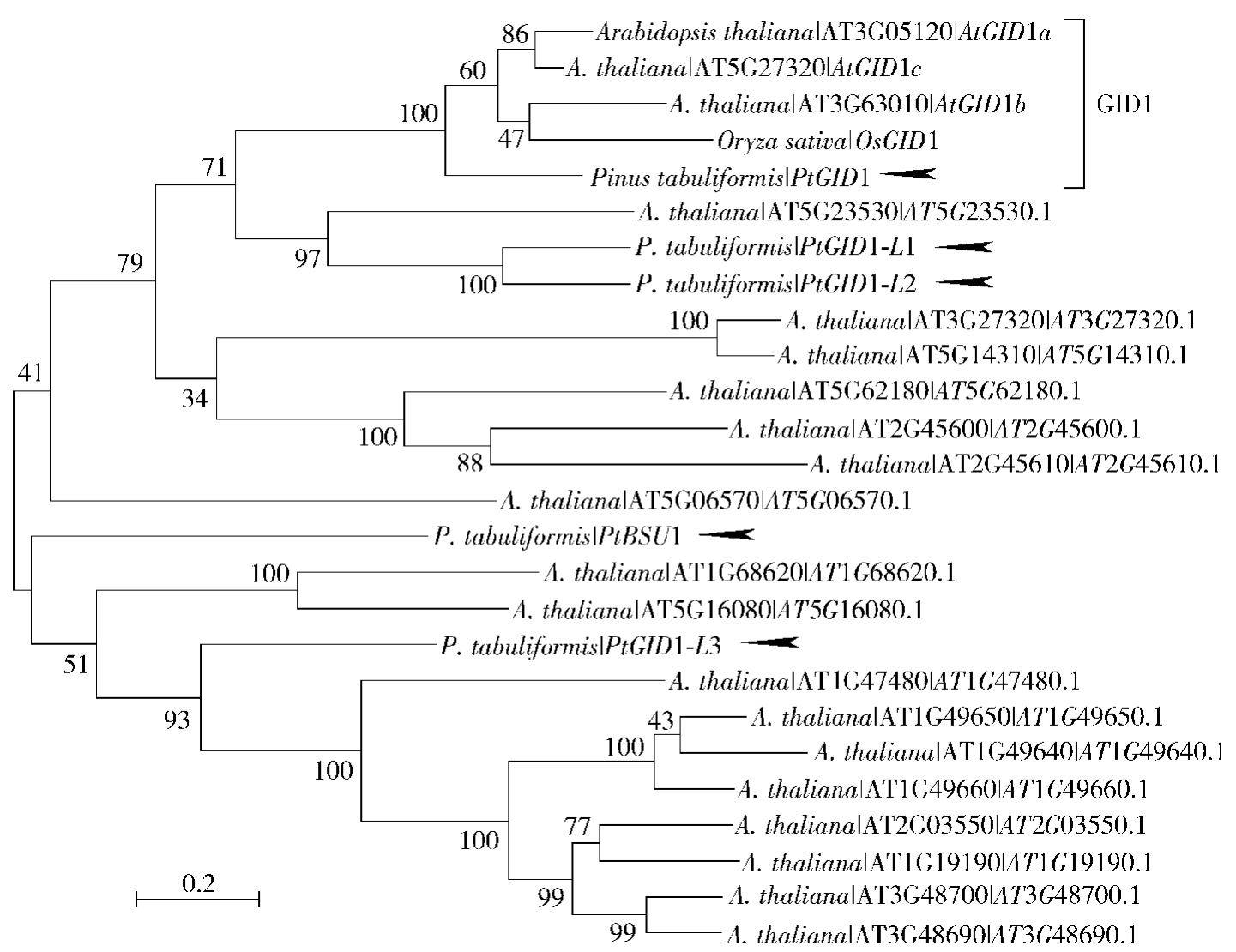
图1 油松与拟南芥GID1-like基因系统发育分析
Fig.1 Phylogenetic analysis of GID1-like genes from Pinus tabuliformis and Arabidopsis thaliana
箭头指示的是在本研究中所克隆的油松GID1相似基因。The arrows indicate GID1-like genes in P. tabuliformis in this study.
上述结果表明,油松全基因组中很可能只有一个GID1同源基因——PtGID1。以其序列为参考,设计通用引物,以樟子松、白皮松、赤松DNA为模板进行克隆测序,结合针叶树公共数据库信息,共获得8种针叶树GID1同源基因序列。这些同源基因全长分别为:白皮松1 565 bp、日本落叶松1 582 bp、白云杉和挪威云杉1 580 bp、油松和火炬松1 599 bp、赤松1 601 bp、樟子松1 604 bp,它们都含有一个内含子和两个外显子,白云杉和挪威云杉GID1编码352个氨基酸残基,日本落叶松GID1编码355个氨基酸残基,其余针叶树GID1基因编码357个氨基酸残基。
2.2 针叶树GID1同源基因的序列分析
对8种针叶树的GID1基因进行序列比对,发现这些基因在针叶树间十分保守。这些基因的DNA序列与被子植物同源基因一样均包含1个内含子(图2),剪切方式符合GT/AG的剪接模式。与外显子序列相比,不同属针叶树GID1内含子变异位点相对较多,但在属内却保持着高度保守性,如油松与挪威云杉内含子间的相似度为85%,而挪威云杉与白云杉内含子序列几乎完全一致,相似度达99%,表明GID1在针叶树中可能对碱基突变非常敏感。

图2 8种针叶树GID1基因内含子序列特征
Fig.2 Characteristics of introns sequence in the GID1 of eight conifers
白色框代表碱基,黑色与灰色条框分别表示相同碱基比例为100%与80%序列;两个箭头间序列为GID1基因内含子。The white frames indicate bases,the black and gray frames indicate the sequences with 100%and 80%similarity bases,respectively.The sequences between two arrows indicate introns in GID1 genes.
将8种针叶树的GID1蛋白序列和江南卷柏、小立碗藓以及水稻、拟南芥等已获得功能验证的GID1蛋白序列进行多重比对(图3),结果显示,这8种针叶树的GID1序列都具有激素敏感性脂肪酶活性区域HGG和GXSXG。和水稻、拟南芥一样,构成HSL家族催化三联体的主要氨基酸(S、D、H)中,S、D在这8种序列中是保守的,而H被I或V取代[11.13]。GID1蛋白与GA或DELLA蛋白有13个结合功能域,从N端到C端依次是TWVLIS、LDR、FFHGGSF、HS、IYD、YRR、DGW、GDSSGGNI、GNI、MF、LDGKYF、WYW和GFY[19]。在8种针叶树中, TWVLIS中的W被F取代,日本落叶松和云杉LDR中的D被E取代,而其他区域都是保守的。自发突变证实与水稻GID1功能相关的3个氨基酸(G169、G196和R251)[20-21]在8种针叶树GID1中都是保守的。对保持水稻GID1的GAs亲和活性必需的17个氨基酸残基[22]在这些序列中都得到了确认,除了白云杉和水稻C-326位的V相同外,其余7种针叶树该位点和AtGID1b、AtGID1c相同,均为I。这些结果表明,针叶树GID1蛋白在GA信号转导中发挥重要功能的氨基酸残基与被子植物一样是保守的,表明它们在GA作用机制中的受体功能可能是完整的。
以8种针叶树和已进行功能验证的部分物种GID1氨基酸序列构建ML进化树,结果如图4所示,GID1基因在进化上的分歧与这些物种进化地位相一致,苔藓、蕨类、被子植物及裸子植物各聚为一类。与被子植物成员相比,针叶树GID1进化速度明显更为缓慢,它们之间积累的差异比拟南芥中3个同源基因成员间的差异还小。GID1在针叶树中的这种极端保守性在进化中的意义有待进行进一步研究。

图3 GID1同源基因氨基酸序列比对
Fig.3 Alignment of amino acid sequences of GID1 homologues
*为GID1蛋白与GA或DELLA蛋白的结合位点,◆为保持GAs亲和活性必需的氨基酸残基,方框为HSL家族蛋白的同源保守序列。*indicates the binding sitesof GA and DELLA proteins in GID1.◆indicates the residues required for GA binding. The conserved sequences of HSL family aremarked by black boxes.
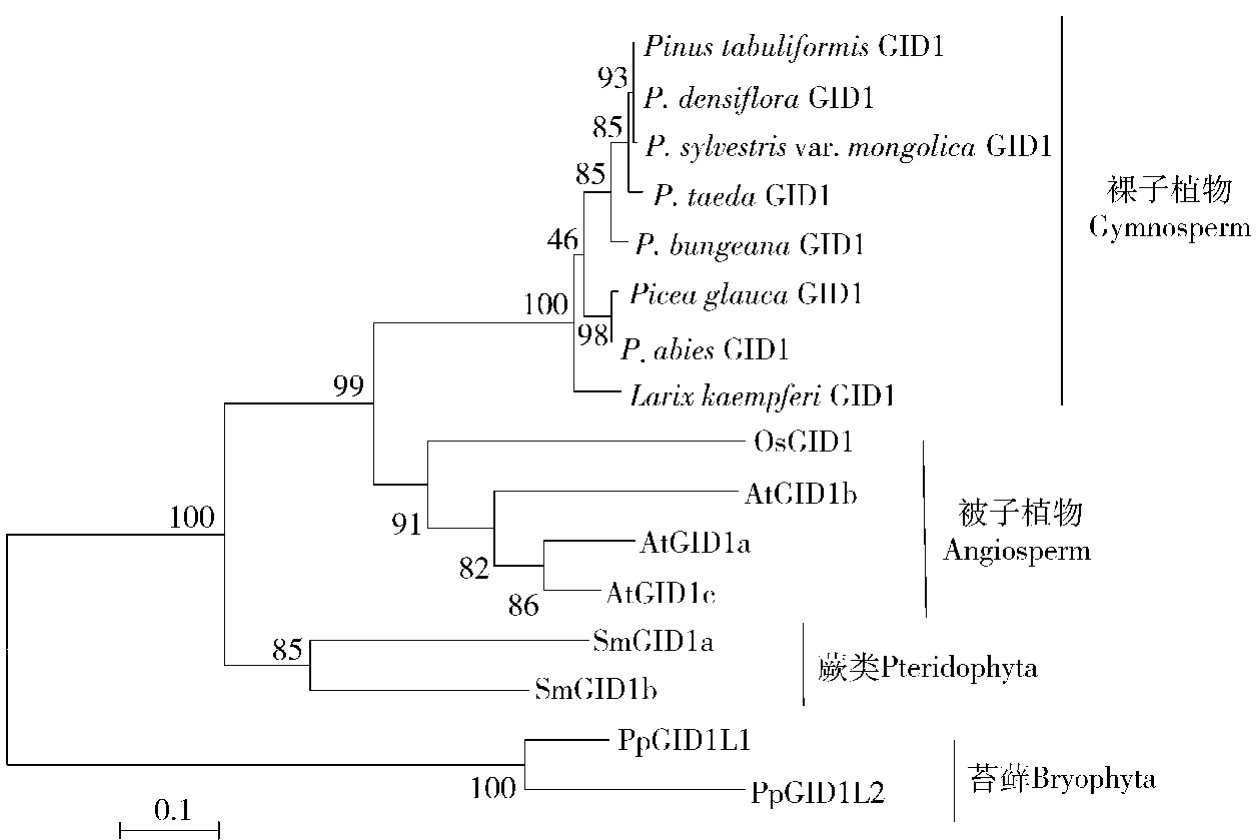
图4 针叶树GID1蛋白与其他GID1蛋白的进化树分析
Fig.4 Unrooted phylogenetic tree of GID1 proteins from conifers and other plants
2.3 针叶树GID1蛋白结构分析
OsGID1和AtGID1a蛋白的晶体结构已经获得了解析,与GA和DELLA蛋白作用的关键位点和结构域都已得到阐述[22-23]。为推测8种针叶树GID1蛋白受体功能的完整性,以OsGID1和AtGID1a蛋白的晶体结构为模板,对油松PtGID1蛋白结构进行了同源建模(图5)。结果表明,油松PtGID1主要结构是由8条β折叠片和7个α螺旋组成的形似袋状的结构,在其N端有两个α螺旋,该结构和水稻OsGID1蛋白的晶体结构十分相似,并且在对GAs的亲和与DELLA蛋白的识别中具有至关重要的作用[22]。但PtGID1在N端比OsGID1多出一个α螺旋(αa),这和AtGID1a的结构相同[23]。OsGID1和AtGID1a的受体功能已经被证实,这也表明本研究中PtGID1与GA潜在结合部位的结构与水稻和拟南芥在进化上是保守的,可能具有相似的功能。
2.4 针叶树GID1基因的表达模式分析
通过云杉基因组数据库(http://congenie.org)数据,对挪威云杉GID1基因(MA_855574g0010)在多个组织中的表达模式进行了分析,结果见图6。云杉GID1在不同组织中均有表达,而且表达水平比较稳定,在所有组织间表达量变化幅度不大,其中在嫩枝顶端的针叶(N4)表达丰度最高,而在木质部(W1)中表达丰度最低,两者间的表达量相比相差最大,仅为1.94倍。这表明这些组织的发育过程均需要GID1及GA信号通路的参与,而生长旺盛的组织可能需要更敏感的GA感受能力,这与GA促进植物生长的生物学功能是一致的。
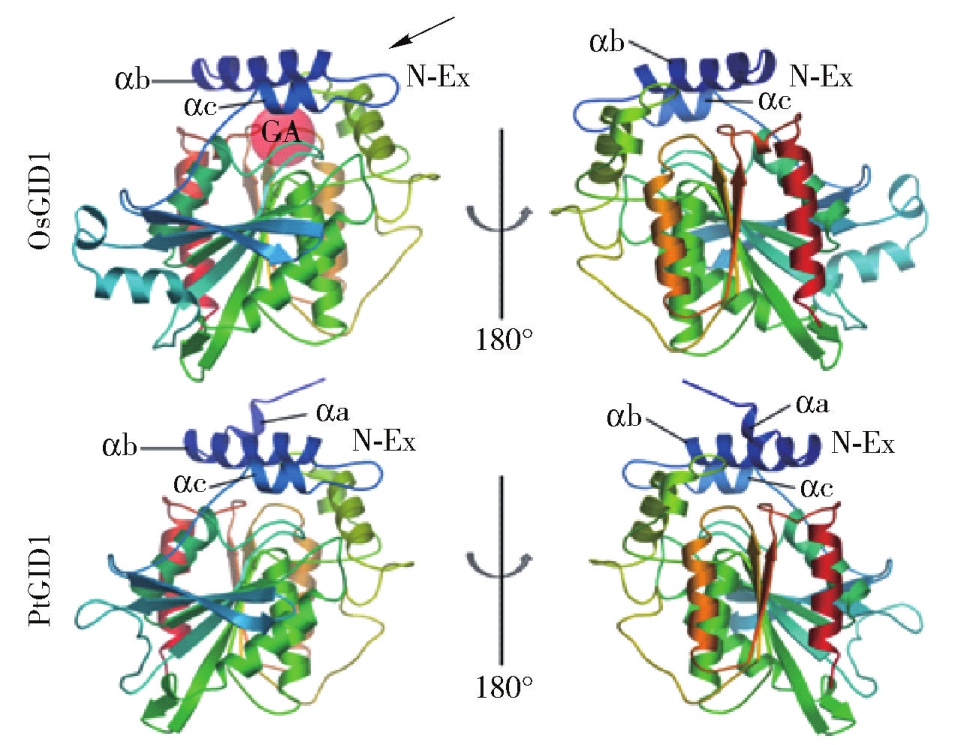
图5 OsGID1蛋白结构及PtGID1的同源建模(E value:2.17×10-129,QMEAN Z-Score:-2.19)
Fig.5 Structure of the OsGID1 and the homologymodeling of PtGID1(E value:2.17×10-129,QMEAN Z-Score:-2.19)
圆球所示的是GA结合部位,箭头所指为GID1结合GA后的N端(N-Ex)状态。The sphere shows the site of GA binding,the arrow indicates the status of N-terminal extension(N-Ex)after GA binding.
研究表明GA在针叶树球花发育过程中具有重要的调控作用,对油松施用GA4/7能促进雌球花发育[24-25]。为了了解GID1在其中的作用,我们对油松营养芽和不同发育阶段的雌雄球花中的GID1表达丰度进行了分析。从图7中可以看出,PtGID1在油松雌雄球花发育过程中的表达和挪威云杉相似,在不同发育阶段间的表达量相比,最大倍数为2.16。在发育初期雌雄球花的相对表达量未及营养芽的2倍,整个发育阶段该基因的表达水平变化幅度不高,表明油松GA信号调控通路中GA受体的转录调控可能并不是核心调控机制,被子植物中GA信号转导调控是通过GID1介导的DELLA蛋白水平的降解实现的,这一机制可能在裸子植物与被子植物分化之前便已经进化获得[26],GID1在针叶树GA作用机制中的作用有待进一步深入研究。
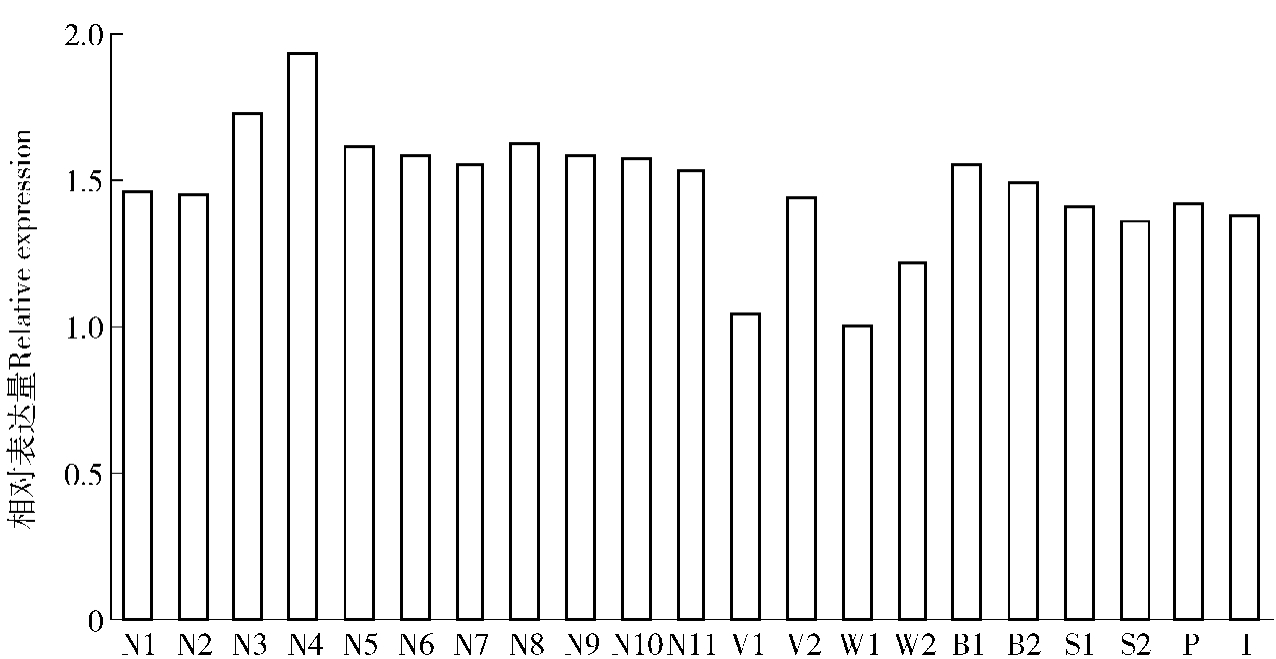
图6 挪威云杉GID1-like基因的相对表达量
Fig.6 Relative expression level of GID1-like gene in Picea abies
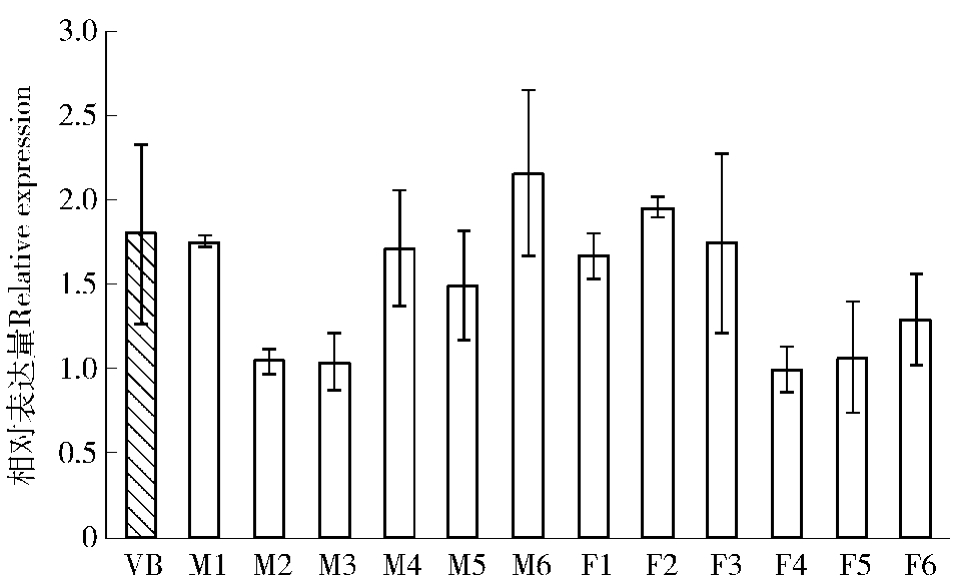
图7 油松雌雄球花不同时期GID1基因的相对表达量
Fig.7 Relative expression level of GID1 gene in P.tabuliformis at different stages
VB为营养芽,M1~M6、F1~F6分别代表雄花和雌花发育的6个时期。VB indicates vegetative bud,M1-M6 and F1-F6 represent male and female cones at six development stages,respectively.
3 结论与讨论
本研究首次在油松全基因组中分离鉴定出了一个GID1直系同源基因,并同源克隆了部分针叶树的GID1同源基因,获得的8种针叶树GID1序列间具有高度的一致性,它们都含有HSL家族的HGG和GXSXG结构域及与GA和DELLA蛋白相结合的作用位点。通过和OsGID1蛋白三级结构的对比表明,PtGID1与OsGID1在GA结合部位非常相似,但在N端与AtGID1a一样比OsGID1多出一个α螺旋(αa)。它们和羧酸酯酶结构相似,不过和其他GID1一样,其N端的62个氨基酸残基形成了特殊的N端延伸(N-Ex),这对赤霉素受体的功能具有重要作用。以上结果表明,和被子植物一样,针叶树GID1基因也是由HSL家族基因衍化而来,其关键结构位点和功能位点具有很高的保守性,它们的结构和功能应该是完整的;因而推测它们可能具有和被子植物GID1相似的GA受体功能。
对挪威云杉和油松不同组织GID1基因的表达模式分析表明,该基因在球花和其他组织中均有表达,并且在两个物种中的表达都较为稳定,虽然生长旺盛的组织略高,但变化幅度不高,表明GID1可能广泛参与这些组织的发育过程,并且其没有明显的组织特异性。这和拟南芥、江南卷柏的表达模式相似[13,19],但和葡萄(Vitisvinifera)、陆地棉(Gossypium hisutum)等植物研究结果不同[27-28],可能是由于这些植物的GID1s功能分化,使其组织特异性增强造成的。水稻和拟南芥中GID1超表达会引起赤霉素超敏感的表型,是由于GID1增强了植物感受GA的能力。对棉花、板栗(Castaneamollissima)等植物外施赤霉素后GID1表达下调[28-29],表明GA和GID1的表达存在反馈调节。因此推测本研究中GID1表达丰度的变化可能和针叶树组织中内源赤霉素含量的变化有关。其表达量变化与GA浓度的关系以及相关的生理作用还需要进一步研究。
虽然松科树种施用GA4、GA7等极性较小的赤霉素能够明显促进其开花和球果发育的现象一直吸引着育种学家的注意,但其作用的分子机制却并不清楚。GID1基因作为赤霉素信号通路的可溶性受体,是赤霉素作用的关键调控因子之一。对辐射松(Pinusradiata)内源GAs含量的测定结果显示,GA3在营养芽和雄花芽中含量虽然相对较高但比较稳定,而GA4则差异明显,特别是雄球花芽中含量变化最大,这也表明GA4可能和它们的发育调节有关[30]。在鉴定拟南芥AtGID1s基因时,Nakajima等[13]发现在供试的活性GAs中,AtGID1s和GA4的亲和力最高,并推测可能是由于GA4是拟南芥中主要的内源GAs,并且是其活性较高的原因。因此GA4调节松科树种发育可能和GA信号通路对其敏感性有关。
参考文献:
[1]MUTASA-GOTTGENSE,HEDDEN P.Gibberellin as a factor in floral regulatory networks[J].Journal of Experimental Botany, 2009,60(7):1979-1989.
[2]PIMENTA L M,KNOP N,LANGE T.Stamen-derived bioactive gibberellin is essential for male flower development ofCucurbita maximaL.[J].Journal of Experimental Botany,2012,63(7): 2681-2691.
[3]OGAWA M,HANADA A,YAMAUCHI Y,et al.Gibberellin biosynthesis and response during Arabidopsis seed germination [J].Plant Cell,2003,15(7):1591-1604.
[4]GABRIELE S,RIZZA A,MARTONE J,et al.The Dof protein DAG1 mediates PIL5 activity on seed germination by negatively regulating GA biosynthetic geneAtGA3ox1[J].The Plant Journal, 2010,61(2):312-323.
[5]李哲馨,钮世辉,高琼,等.赤霉素调控木质部发育的细胞学研究[J].北京林业大学学报,2014,36(2):68-73.
LI Z X,NIU S H,GAO Q,et al.Cytological study of gibberellin regulated xylem development[J].Journal of Beijing Forestry University,2014,36(2):68-73.
[6]盛楚兴.针叶树的阶段转变及成花诱导研究现状[J].北京林业大学学报,1986,8(1):110-123.
SHENG C X.The current researches on developmental phase transitions and floral induction in conifers[J].Journal of Beijing Forestry University,1986,8(1):110-123.
[7]PHARIS R P,WEBBER J E,ROSS S D.The promotion of flowering in forest treesby gibberellin A4/7and cultural treatments: a review of the possible mechanisms[J].Forest Ecology and Management,1987,19(1):65-84.
[8]江玲,周燮,王章荣,等.马尾松雌雄球花的形成与赤霉素和脱落酸及细胞分裂素的关系[J].南京林业大学学报:自然科学版,1998,22(3):61-65.
JIANG L,ZHOU X,WANG Z R,et al.Relationship between the formation ofmale or female strobili and the levels of GAs,ABA, CTKs in Masson pine[J].Journal of Nanjing Forestry University: Natural Science Edition,1998,22(3):61-65.
[9]ALMQVIST C.Timing of GA4/7application and the flowering ofPinus sylvestrisgrafts in the greenhouse[J].Tree Physiology, 2003,23(6):413-418.
[10]SHEARER R C,STOEHR M U,WEBBER JE,et al.Seed cone production enhanced by injecting 38-year-oldLarix occidentalisNutt.with GA4/7[J].New Forests,1999,18(3):289-300.
[11]UEGUCHI-TANAKA M,ASHIKARI M,NAKAJIMA M,et al. Gibberellin insensitive dwarf 1 encodes a soluble receptor for gibberellin[J].Nature,2005,437:693-698.
[12]UEGUCHI-TANAKA M,NAKAJIMA M,MOTOYUKI A,et al. Gibberellin receptor and its role in gibberellin signaling in plants [J].Annual Review of Plant Biology,2007,58:183-198.
[13]NAKAJIMA M,SHIMADA A,TAKASHI1 Y,et al.Identification and characterization of Arabidopsis gibberellin receptors[J].The Plant Journal,2006,46(5):880-889.
[14]EDGAR R C.Muscle:amultiple sequence alignmentmethod with reduced time and space complexity[J].BMC Bioinformatics, 2004,5(1):113.
[15]EDGAR R C.Muscle:multiple sequence alignment with high accuracy and high throughput[J].Nucleic Acids Research,2004, 32(5):1792-1797.
[16]ARNOLD K,BORDOLI L,KOPP J,et al.The swiss-model workspace:a web-based environment for protein structure homologymodeling[J].Bioinformatics,2006,22(2):195-201.
[17]KIM D,SALZBERG SL.Tophat-fusion:an algorithm for discovery of novel fusion transcripts[J].Genome Biology,2011,12(8): R72.
[18]TRAPNELL C,PACHTER L,SALZBERG S L.Tophat: discovering splice junctions with RNA-Seq[J].Bioinformatics, 2009,25(9):1105-1111.
[19]HIRANO K,NAKAJIMA M,ASANO K,et al.The GID1-mediated gibberellin perception mechanism is conserved in the lycophyteSelaginella moellendorffiibut not in the bryophytePhyscomitrella patens[J].The Plant Cell,2007,19(10):3058-3079.
[20]HIRANO K,UEGUCHI-TANAKA M,MATSUOKA M.GID1-mediated gibberellin signaling in plants[J].Trends in Plant Science,2008,13(4):192-199.
[21]UEGUCHI-TANAKA M,NAKAJIMA M,KATOH E,et al. Molecular interactions of a soluble gibberellin receptor,GID1,with a rice DELLA protein,SLR1,and gibberellin[J].The Plant Cell, 2007,19(7):2140-2155.
[22]SHIMADA A,UEGUCHI-TANAKA M,NAKATSU T,et al. Structural basis for gibberellin recognition by its receptor GID1 [J].Nature,2008,456:250-253.
[23]MURASE K,HIRANO Y,SUN T P,et al.Gibberellin-induced DELLA recognition by the gibberellin receptor GID1[J].Nature, 2008,456:459-464.
[24]SHENG C,WANG S.Effect of applied growth regulators and cultural treatments on flowering and shoot growth ofPinus tabulaeformis[J].Canadian Journal of Forest Research,1990,20 (6):679-685.
[25]ZHAO P,FAN J,ZHANG S,et al.Effects of gibberellins A4/7,6-benzylaminopurine and chlormequat chloride on the number of male and female strobili and immature cones in Chinese pine(Pinus tabuliformis)with foliar sprays[J].Journal of Forestry Research,2011,22(3):353-359.
[26]WANG Y,DENG D.Molecular basis and evolutionary pattern of GA-GID1-DELLA regulatory module[J].Mol Genet Genomics, 2014,289(1):1-9.
[27]金良,葛晖,陈尚武,等.2个葡萄GID(gibberellin insensitive dwarf)基因的克隆与表达[J].中国农业大学学报,2013, 18(4):64-70.
JIN L,GE H,CHEN SW,et al.Cloning and expression analysisof two grapeGID(gibberellin insensitive dwarf)genes[J].Journal of China Agricultural University,2013,18(4):64-70.
[28]董静,尹梦回,杨帆,等.棉花赤霉素不敏感矮化GID1同源基因的克隆和表达分析[J].作物学报,2009,35(10):1822-1830.
DONG J,YIN M H,YANG F,et al.Cloning and expression profiling of gibberellin insensitive dwarfGID1 homologous genes from cotton[J].Acta Agronomica Sinica,2009,35(10):1822-1830.
[29]李兴亮,郭献平,沈元月,等.板栗赤霉素缺陷型短雄花序芽变的初步鉴定及CmGID1基因的表达分析[J].园艺学报,2011, 38(7):1251-1258.
LIX L,GUO X P,SHEN Y Y,et al.Preliminary identification of GAs-deficient shortmale catkin mutant and expression analysis ofCmGID1 inCastanea mollissima[J].Acta Horticulturae Sinica, 2011,38(7):1251-1258.
[30]FERNANDEZ H,FRAGA M,BERNARD P,etal.Quantification of GA1,GA3,GA4,GA7,GA9,and GA20in vegetative andmale cone buds from juvenile and mature trees ofPinus radiata[J].Plant Growth Regulation,2003,40(3):185-188.
(责任编辑 赵 勃 董晓燕 责任编委 苏晓华 诸葛强)
Isolation and identification of GID1 orthologous gene in conifers and its function prediction.
Key words:gibberellins;conifers;GID1 gene;isolation and identification;function prediction
中图分类号:S718.46
文献标志码:A
文章编号:1000-1522(2015)05-0040-09
DOI:10.13332/j.1000-1522.20140255
收稿日期:2014-07-21
修回日期:2014-12-08
基金项目:国家自然科学基金项目(31370657)、“948”国家林业局引进项目(2012-4-40)。
GID1 as the gibberellins(GA)receptor is an essential component of GA signaling pathway.TheGID1 genes have been cloned widely from angiosperms,but researches on them in conifers are scarcely documented.We obtained and identified the orthologous gene ofGID1 fromPinustabuliformistranscriptome withAtGID1sprobe sequence.Based on this sequence,theGID1 geneswere cloned fromP. sylvestrisvar.mongolica,P.bungeanaandP.densifloraand theGID1-likegenes inP.taeda,Picea glauca,P.abiesandLarixkaempferiwere also obtained from public database.The conservation of amino acid sequences,protein structures and expression levels of coniferousGID1swere analyzed.The result showed that there probably is only oneGID1 with highly conserved sequence in conifers.Although the identity ofGID1sis low between conifers and angiosperms,they have highly similar amino acidswhich are essential for binding affinity to GA and quite conserved functional domains which can interact with DELLA protein.Thus,these orthologousGID1 genesmay have functions of receptor.Expression analysis showed that theGID1 had stable expressions in different organs inP.abiesand in different developmental stages ofmale and female cones inPinustabuliformis,indicating thatGID1 may widely participate in developmental process of these tissues,and the transcriptional regulation ofGID1 might not be the key regulatorymechanism in GA signaling pathway.Our study lays a foundation for the research ofmolecularmechanism ofGID1 in the growth and development of conifers.

