ZN~(2+)胁迫对白皮松针叶电阻抗图谱参数的影响
【类型】期刊
【作者】周军,张钢,刘晓红,姚琳(河北农业大学园艺学院;延安大学化学与化工学院)
【作者单位】河北农业大学园艺学院;延安大学化学与化工学院
【刊名】沈阳农业大学学报
【关键词】 电阻抗参数;细胞膜;重金属离子;白皮松
【资助项】河北农业大学留学回国人员启动基金项目 (200406)
【ISSN号】1000-1700
【页码】P667-672
【年份】2019
【期号】第6期
【期刊卷】1;|7;|8;|4;|5
【摘要】研究了Zn2+胁迫下白皮松(Pinus bungeana)针叶细胞膜的电特性,对盆栽6a生白皮松苗,应用电阻抗图谱法测定了不同浓度Zn2+(0,200,500,1000,2000,3000 mg.L-1)胁迫下白皮松针叶的胞外电阻率、胞内电阻率、弛豫时间、弛豫时间分布系数、高频电阻率和低频电阻率。结果表明:在Zn2+胁迫下,随处理时间的延长,胞外电阻率和低频电阻率总是增加,胞内电阻率和高频电阻率则先减小后增加,弛豫时间先增加后减小,弛豫时间分布系数无明显变化趋势。随Zn2+胁迫浓度的增加,处理7d后各参数均无明显变化;处理14d后,各参数均随浓度的增加逐渐增加,相比对照,胞外电阻率和低频电阻率都分别增加了115%235%,胞内电阻率分别增加了34%95%;处理21d后,除弛豫时间分布系数外,其余各参数在3000mg.L-1Zn2+处理相比对照差异显著,胞外电阻率和低频电阻率增加129%,胞内电阻率增加232%,弛豫时间减少74%,高频电阻率增加216%;处理28d后,胞外电阻率、胞内电阻率、高频电阻率和低频电阻率均在Zn2+浓度200,2000,3000 mg.L-1时与对照相比有显著差异。可见,Zn2+胁迫处理14d时,对白皮松针叶均有明显伤害,可能是对Zn2+胁迫最敏感时期;白皮松针叶不能忍耐2000 mg.L-1以上Zn2+浓度胁迫。
【全文】 文献传递
Zn2+胁迫对白皮松针叶电阻抗图谱参数的影响
摘要:研究了Zn2+胁迫下白皮松(Pinus bungeana)针叶细胞膜的电特性,对盆栽6a生白皮松苗,应用电阻抗图谱法测定了不同浓度 Zn2+(0,200,500,1000,2000,3000 mg·L-1)胁迫下白皮松针叶的胞外电阻率、胞内电阻率、弛豫时间、弛豫时间分布系数、高频电阻率和低频电阻率。结果表明:在Zn2+胁迫下,随处理时间的延长,胞外电阻率和低频电阻率总是增加,胞内电阻率和高频电阻率则先减小后增加,弛豫时间先增加后减小,弛豫时间分布系数无明显变化趋势。随Zn2+胁迫浓度的增加,处理7d后各参数均无明显变化;处理14d后,各参数均随浓度的增加逐渐增加,相比对照,胞外电阻率和低频电阻率都分别增加了115% ~235%,胞内电阻率分别增加了34% ~95%;处理21d后,除弛豫时间分布系数外,其余各参数在3000mg·L-1Zn2+处理相比对照差异显著,胞外电阻率和低频电阻率增加129%,胞内电阻率增加232%,弛豫时间减少74%,高频电阻率增加216%;处理28d后,胞外电阻率、胞内电阻率、高频电阻率和低频电阻率均在Zn2+浓度200,2000,3000 mg·L-1时与对照相比有显著差异。可见,Zn2+胁迫处理14d时,对白皮松针叶均有明显伤害,可能是对Zn2+胁迫最敏感时期;白皮松针叶不能忍耐2000 mg·L-1以上Zn2+浓度胁迫。
关键词:电阻抗参数;细胞膜;重金属离子;白皮松
随着经济的发展,工业“三废”的排放日益增多,使环境中重金属污染日益严重[1]。研究表明,重金属不仅影响植物根系对矿质养分的吸收和运输,导致植物的营养缺乏,还能诱导植物体内的氧化胁迫,引起膜脂过氧化。进入细胞内的重金属离子与酶活性中心或蛋白质的巯基结合,取代金属蛋白中的必需元素,而导致生物大分子构象改变,造成酶活性下降、丧失,干扰细胞的正常代谢活动[2-3]。这些研究往往集中在重金属对植物生长发育的外在表型、内部结构及过氧化胁迫等生理生化的影响方面[4],有关重金属胁迫引起植物细胞膜电特性变化的研究很少。电阻抗图谱(electrical impedance spectroscopy,EIS)是将特定的生物细胞或组织放在交流电场中,产生的电阻和电抗在复平面内随频率变化形成的曲线。研究这种通过等效电路拟合得到的电阻抗图谱参数对生物组织生理变化的响应被称为电阻抗图谱法。EIS能够获得待测植物组织和器官的基本生理学信息[5],在国外已被广泛地用于估测植物活力[6]、养分状况[7]、果实受害程度[8]、抗寒性[9-10]等。在所有这些研究中,EIS法提供了非破坏性地测定胞内电阻、胞外电阻和膜变化的手段。其中,应用EIS法估测植物的抗寒性方面做了大量工作。EIS法在植物抗逆性研究中,比较容易、快速,是一种有效实用的物理方法。白皮松(Pinus bungeana)属于松科松属常绿乔木,针叶3针1束,是一种优良的绿化和造林树种,广泛栽培于我国许多城市的公园和道路两侧。本试验采用不同浓度的重金属离子Zn2+对白皮松进行处理,当Zn2+胁迫引起植物组织的细胞膜发生变化时,这种变化就可以通过EIS参数记录下来。在理想情况下,EIS参数对不同浓度的胁迫应该有一定的响应,就可以考虑用EIS参数来诊断白皮松受重金属胁迫的程度。通过本试验研究,试图建立一种新的检测重金属离子含量影响植物抗性的方法,对环境中有害物质的分析具有方法创新的重要意义。
1 材料与方法
1.1 材料
供试白皮松 6a生实生苗,取自北京十三陵林场昊林苗圃(40°44′N,116°35′E),挑选生长正常且大小相近的苗木于2009年4月2日移栽入河北农业大学(河北省保定市,38°50′N,115°26′E)温室进行缓苗。供试化学试剂ZnSO4·7H2O(天津市福晨化学试剂厂生产)为分析纯,含量不少于99.5%。
1.2 试验设计
本试验采用盆栽方法,盆长40 cm,宽28 cm,深15 cm。基质为沙子∶蛭石=2∶1,充分混合,并使每盆所装基质相近。每盆种6株白皮松,每个处理3盆,即3次重复。缓苗期间14d浇1次营养液,营养液配方为园式配方(硝酸钙 950 mg·L-1,硝酸钾 810 mg·L-1,磷酸二氢铵 155 mg·L-1,硫酸镁 500 mg·L-1,硼酸 3 mg·L-1,硫酸锰 2 mg·L-1,硫酸锌 0.22 mg·L-1,硫酸铜 0.05 mg·L-1,钼酸铵 0.02 mg·L-1,螯合铁 20 mg·L-1),7d 浇 1 次水。试验设计ZnSO4浓度分别为0(清水对照),200,500,1000,2000,3000 mg·L-1共6个处理,5月24日进行Zn2+胁迫处理,处理后采用相同的水分管理和养分管理。每次取样每个处理从每盆取1株苗进行电阻抗的测定。分别在处理7 d(5月 31 日)、14 d(6 月 7 日)、21 d(6 月 14 日)、28 d(6 月 21 日)后取样进行指标测定。
1.3 测定项目及方法
1.3.1 白皮松针叶电阻抗参数的测定 取样后,样本马上装入塑料袋、封口,放于盛有冰块的保鲜盒中[11]。白皮松针叶的电阻、电抗测定参考ZHANG等[9]的方法。首先将Ag/AgCl电极与阻抗分析仪(HP4284A,Agilent,USA)相连,将电极插入玻璃管,把凝胶分别挤进支撑样本的2个水平玻璃管中。然后将经过不同处理的针叶切取中部15mm,测定叶片的厚度,把样本放置在2个玻璃管之间,通过电极接触凝胶,再通过凝胶轻轻接触待测样本,在测定过程保持样本的原初状态不变以保证测定结果的稳定性。对阻抗分析仪进行开路和短路校正。校正后分别测定样本在42个频率下的电阻值和电抗值,测定频率范围为80 ~1000000Hz,输入电压为20mV。
1.3.2 等效电路的确定及电阻抗图谱参数的拟合 将上述频率下测定样本的电阻和电抗值分别作为实部和虚部绘出各个频点的变化曲线,即电阻抗图谱。根据电阻抗图谱确定样本适用的等效电路。植物一般使用两种类型的等效电路:集总模型和分布模型,究竟应用哪种模型,取决于电阻抗图谱弧的数量和图谱的偏度[9]。白皮松针叶的电阻抗图谱是一个单一的弧,并且有一个凹陷中心,因此针叶叶肉细胞用模型A。在该模型中阻抗的表达式为:Zmodel-A=R∞+[(R0-R∞)·(1+β)]/[1+β·(1+j·ω·τm)0.5]。式中:R∞ 和 R0分别是在极高频与极低频下的电阻;τm是细胞膜的时间恒量,τm=R3×Cm,其中R3和Cm分别为细胞膜的电阻及电容;系数β是控制图谱偏度及凹陷中心的一个因子;j=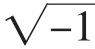 ,是复数算符(complex number operator);ω=2×π×f,是角速度(f为交流电频率)[9]。 等效电路参数 R∞、R0、τm和 β 应用 Repo发展了的 LEVMV.6 (J.R.Macdonald,Department of Physics and Astronomy,University of North Carolina,Chapel Hill,NC)软件进行拟合[12]。
,是复数算符(complex number operator);ω=2×π×f,是角速度(f为交流电频率)[9]。 等效电路参数 R∞、R0、τm和 β 应用 Repo发展了的 LEVMV.6 (J.R.Macdonald,Department of Physics and Astronomy,University of North Carolina,Chapel Hill,NC)软件进行拟合[12]。
低频电阻 R0对应于胞外电阻 Re,而胞内电阻 Ri=R∞·R0/(R0-R∞)。
根据每一个样本的截面积和长度,将得到的胞外和胞内电阻归一化,计算样本的电阻率。再根据每个样本的截面积、长度和高频电阻与低频电阻计算得出高频电阻率和低频电阻率。电阻率rx=Rx·A/l。式中:rx的单位为Ωm;Rx是测定的电阻,单位为Ω;A是样本的横切面面积,单位为m2;l是样本长度,单位为m[9]。白皮松针叶的横切面被看作是圆心角为60°的扇形,故A=π×d2/3,式中:d表示针叶的厚度,样本长度l为15mm。
弛豫时间和弛豫时间分布系数不作归一化处理[13]。
试验所得数据采用SPSS17.0对数据进行处理和方差分析。
2 结果与分析
2.1 不同浓度Zn2+胁迫下白皮松针叶胞外电阻率和低频电阻率的变化
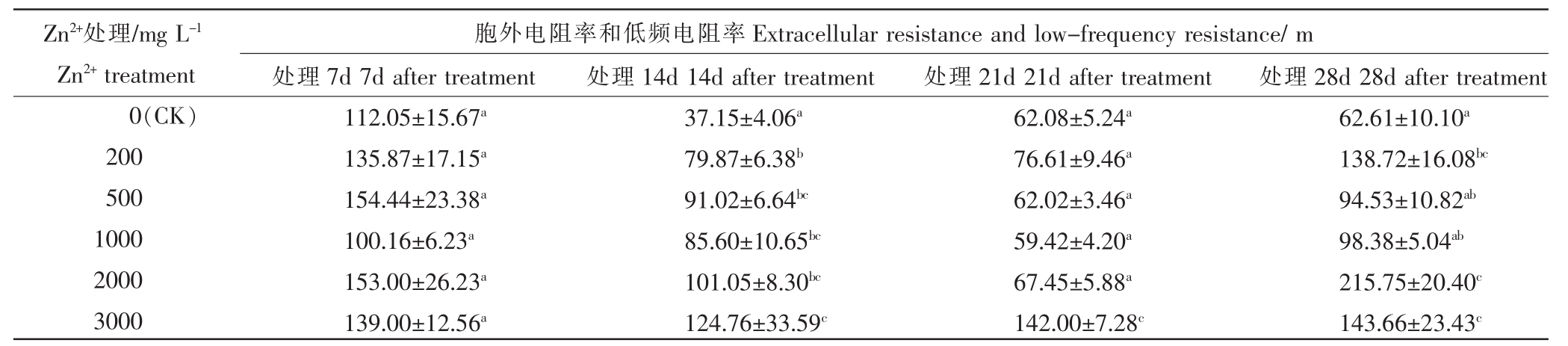
由表1可知,Zn2+处理7d后,胞外电阻率相比对照均有所增加,但均无显著差异;处理14d后各浓度处理白皮松针叶的胞外电阻率相比对照均有所增加,增加了115%~235%,除1000 mg·L-1Zn2+处理略低于500 mg·L-1Zn2+处理,其余随浓度的升高逐渐增加,且均有显著差异(p<0.05),3000 mg·L-1Zn2+处理相比对照差异达到极显著水平(p<0.01);21d 后 3000 mg·L-1Zn2+处理与对照相比有极显著差异(p<0.01),相比对照增加 129%;28d后 500 mg·L-1Zn2+处理和 1000 mg·L-1Zn2+处理与对照相比无显著差异,2000 mg·L-1和 3000 mg·L-1Zn2+处理与对照相比有极显著差异(p<0.01),200 mg·L-1处理与对照相比有显著差异(p<0.05)。 可见, Zn2+处理 7d 后胞外电阻率变化不大,说明白皮松还没有受害。处理14d后,各浓度Zn2+处理的胞外电阻率相比对照均有较大变化,说明白皮松已经受害,尤其是高浓度(3000 mg·L-1)时受害最大;处理21~28d后低浓度Zn2+处理白皮松可能已经开始适应,但高浓度继续受害。由于低频电阻率与胞外电阻率值相同,所以低频电阻率和胞外电阻率变化趋势一样。
表1 不同浓度Zn2+胁迫下白皮松针叶的胞外电阻率和低频电阻率
Table 1 The extracellular resistance and low-frequency resistance of Pinus bungeana needles under different concentrations of Zn2+stress
注:表中同列中,a与b不同表示差异显著(p<0.05),a与c不同表示差异极显著(p<0.01)。表中数据为均值±标准误。下同。
Note:In the same column,a and b refer to significant different at level of p<0.05;a and c refer to significant difference at level of p<0.01.Data in the table:Mean±standard error of mean.The same below.
Zn2+处理/mg L-1 Zn2+treatment 0(CK)200 500 1000 2000 3000胞外电阻率和低频电阻率Extracellular resistance and low-frequency resistance/m处理7d 7d after treatment 112.05±15.67a 135.87±17.15a 154.44±23.38a 100.16±6.23a 153.00±26.23a 139.00±12.56a处理14d 14d after treatment 37.15±4.06a 79.87±6.38b 91.02±6.64bc 85.60±10.65bc 101.05±8.30bc 124.76±33.59c处理21d 21d after treatment 62.08±5.24a 76.61±9.46a 62.02±3.46a 59.42±4.20a 67.45±5.88a 142.00±7.28c处理28d 28d after treatment 62.61±10.10a 138.72±16.08bc 94.53±10.82ab 98.38±5.04ab 215.75±20.40c 143.66±23.43c
2.2 不同浓度Zn2+胁迫下白皮松针叶胞内电阻率的变化
由表2可知,Zn2+处理7d后,各浓度处理的胞内电阻率和对照相比均有所降低,但无显著差异,各浓度处理间也无差异;14d后Zn2+浓度处理为200~2000 mg·L-1时,胞内电阻率随Zn2+浓度的升高逐渐增加,增加了34%~95%,3000mg·L-1Zn2+处理仅比对照增加 34%,2000 mg·L-1Zn2+处理与对照相比有显著差异(p<0.05),其余均无差异;21d后3000mg·L-1Zn2+处理与对照相比有极显著差异(p<0.01),相比对照增加232%,其余均无差异;28d 后与对照相比胞内电阻率均有增加,200 mg·L-1Zn2+处理与对照相比有显著差异 (p<0.05),2000 mg·L-1Zn2+处理有极显著差异(p<0.01)。综合可知,相比对照,胞内电阻率随处理时间的延长有先降低后增加的趋势。
2.3 不同浓度Zn2+胁迫下白皮松针叶弛豫时间的变化
由表3可知,Zn2+处理7d后,各浓度处理的弛豫时间和对照相比均无显著差异,各浓度间也无显著差异,但弛豫时间均高于对照,且随浓度的升高逐渐减低;14d后各Zn2+浓度处理均高于对照,除3000 mg·L-1Zn2+处理与对照相比有显著差异(p<0.05),其余均无显著差异;21d后除500 mg·L-1Zn2+处理高出对照3%,其余均低于对照,3000 mg·L-1Zn2+处理和对照有显著差异(p<0.05),相比对照减少 74%,其余均无显著差异;28d 后各 Zn2+浓度处理均低于对照,但无显著差异,各浓度间也无显著差异。综上可见,随处理时间的变化,弛豫时间相比对照是先增加后减小的趋势;随Zn2+浓度的变化,弛豫时间没有明显的变化趋势,除处理7d后,高浓度相比对照有较大的变化幅度,而低浓度变化幅度较小。
表2 不同浓度Zn2+胁迫下白皮松针叶的胞内电阻率
Table 2 The intracellular resistance of Pinus bungeana needles under different concentrations of Zn2+stress
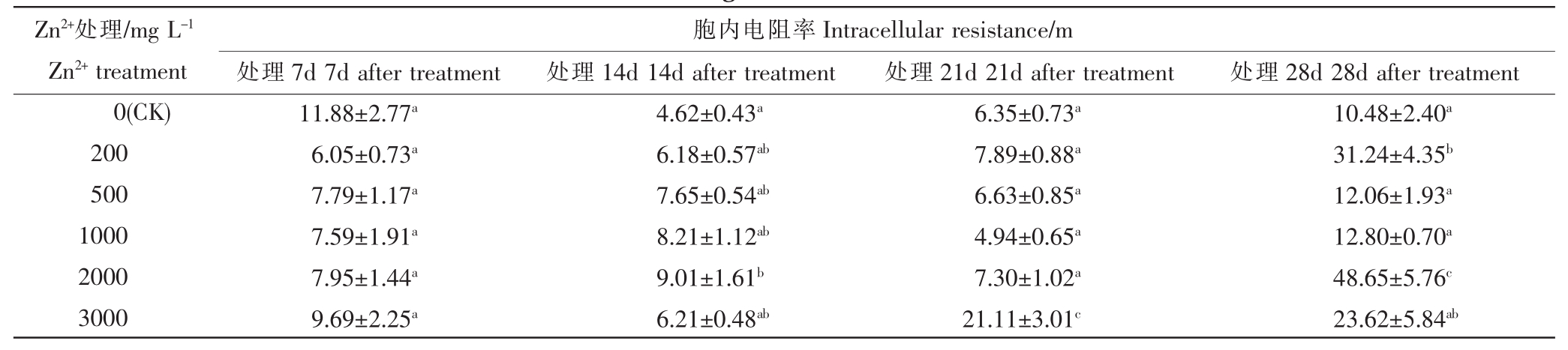
Zn2+处理/mg L-1 Zn2+treatment 0(CK)200 500 1000 2000 3000处理7d 7d after treatment 11.88±2.77a 6.05±0.73a 7.79±1.17a 7.59±1.91a 7.95±1.44a 9.69±2.25a胞内电阻率Intracellular resistance/m处理14d 14d after treatment 4.62±0.43a 6.18±0.57ab 7.65±0.54ab 8.21±1.12ab 9.01±1.61b 6.21±0.48ab处理21d 21d after treatment 6.35±0.73a 7.89±0.88a 6.63±0.85a 4.94±0.65a 7.30±1.02a 21.11±3.01c处理28d 28d after treatment 10.48±2.40a 31.24±4.35b 12.06±1.93a 12.80±0.70a 48.65±5.76c 23.62±5.84ab
表3 不同浓度Zn2+胁迫下白皮松针叶的弛豫时间
Table 3 Relaxation time of Pinus bungeana needles under different concentrations of Zn2+stress
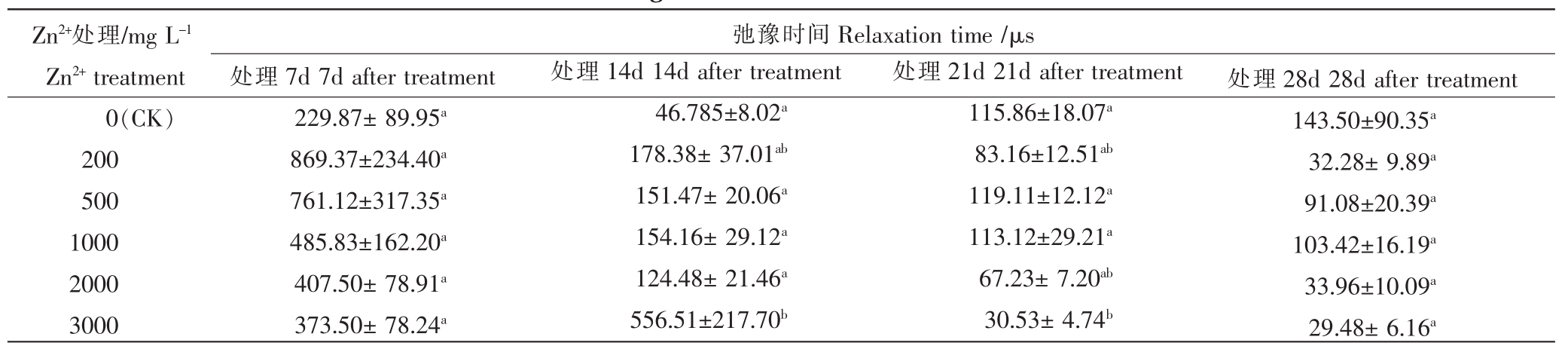
Zn2+处理/mg L-1 Zn2+treatment 0(CK)200 500 1000 2000 3000处理7d 7d after treatment 229.87±89.95a 869.37±234.40a 761.12±317.35a 485.83±162.20a 407.50±78.91a 373.50±78.24a弛豫时间Relaxation time/μs处理14d 14d after treatment 46.785±8.02a 178.38±37.01ab 151.47±20.06a 154.16±29.12a 124.48±21.46a 556.51±217.70b处理21d 21d after treatment 115.86±18.07a 83.16±12.51ab 119.11±12.12a 113.12±29.21a 67.23±7.20ab 30.53±4.74b处理28d 28d after treatment 143.50±90.35a 32.28±9.89a 91.08±20.39a 103.42±16.19a 33.96±10.09a 29.48±6.16a
2.4 不同浓度Zn2+胁迫下白皮松针叶弛豫时间分布系数的变化
由表4可知,各浓度处理的白皮松针叶弛豫时间分布系数相比对照均无显著差异。但处理14d后,除2000 mg·L-1Zn2+处理略低于 1000 mg·L-1Zn2+处理,其余随浓度的增加弛豫时间分布系数逐渐增加,且 3000 mg·L-1Zn2+处理相比对照增加 55%; 处理 21d 后 200 mg·L-1Zn2+处理、500 mg·L-1Zn2+处理和 1000 mg·L-1Zn2+处理与对照相比差异不大,2000 mg·L-1Zn2+处理和3000 mg·L-1Zn2+处理分别比对照高出91%和43%。 处理7d和28d均无显著变化趋势,这和弛豫时间变化相同。
表4 不同浓度Zn2+胁迫下白皮松针叶的弛豫时间分布系数
Table 4 Distribution coefficient of relaxation time of Pinus bungeana needles under different concentrations of Zn2+stress

Zn2+处理/mg L-1 Zn2+treatment(CK)200 500 1000 2000 3000弛豫时间分布系数Distribution coefficient of relaxation time处理7d 7d after treatment 1.41±0.59a 0.59±0.03a 0.74±0.11a 1.81±0.82a 0.66±0.08a 1.67±0.65a处理14d 14d after treatment 0.64±0.01a 0.63±0.03a 0.67±0.01a 0.75±0.04a 0.69±0.03a 0.99±0.22a处理21d 21d after treatment 0.65±0.02a 0.78±0.01a 0.65±0.02a 0.65±0.03a 1.24±0.47a 0.93±0.04a处理28d 28d after treatment 1.43±0.62a 1.26±0.08a 1.73±0.58a 1.37±0.43a 1.24±0.05a 1.40±0.13a
2.5 不同浓度Zn2+胁迫下白皮松针叶高频电阻率的变化
由表5可知,Zn2+处理7d后,各Zn2+浓度处理相比对照有所降低,但无显著差异;14d后Zn2+处理相比对照都有所增加,且随浓度的升高高频电阻率逐渐增加,3000 mg·L-1Zn2+处理相比对照有显著差异(p<0.05),其余无显著差异;21d 后,200~2000 mg·L-1Zn2+处理以下相比对照无显著差异,3000 mg·L-1Zn2+处理显著高于对照 (p<0.05),高于对照 216%;28d 后无明显变化规律,除了 2000 mg·L-1Zn2+处理相比对照有极显著差异(p<0.01),其余均无显著差异。
表5 不同浓度Zn2+胁迫下白皮松针叶的高频电阻率
Table 5 High-frequency resistance of Pinus bungeana needles under different concentrations of Zn2+stress
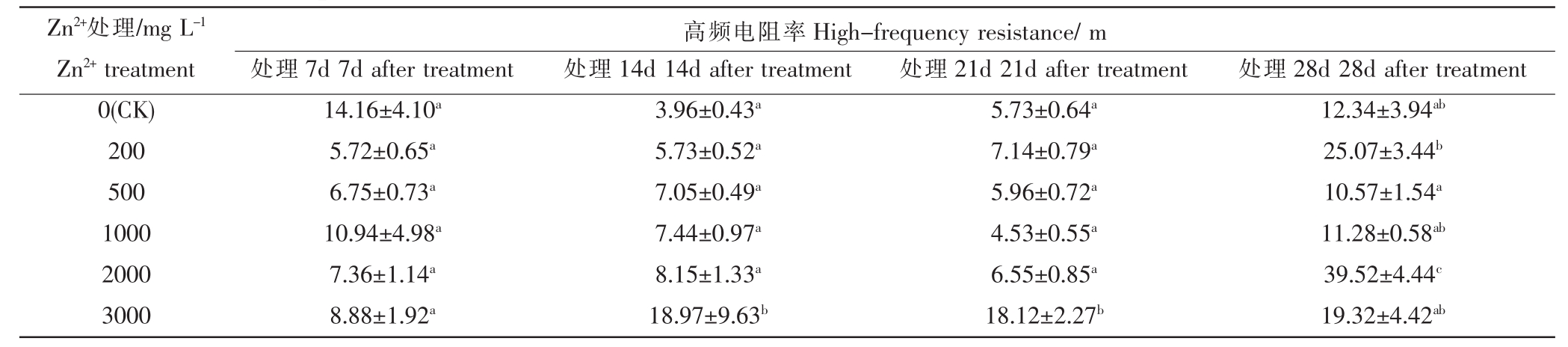
Zn2+处理/mg L-1 Zn2+treatment 0(CK)200 500 1000 2000 3000高频电阻率High-frequency resistance/m处理7d 7d after treatment 14.16±4.10a 5.72±0.65a 6.75±0.73a 10.94±4.98a 7.36±1.14a 8.88±1.92a处理14d 14d after treatment 3.96±0.43a 5.73±0.52a 7.05±0.49a 7.44±0.97a 8.15±1.33a 18.97±9.63b处理21d 21d after treatment 5.73±0.64a 7.14±0.79a 5.96±0.72a 4.53±0.55a 6.55±0.85a 18.12±2.27b处理28d 28d after treatment 12.34±3.94ab 25.07±3.44b 10.57±1.54a 11.28±0.58ab 39.52±4.44c 19.32±4.42ab
3 结论与讨论
研究结果表明,在各浓度Zn2+胁迫下,随处理时间的延长,胞外电阻和低频电阻率总是增加,胞内电阻和高频电阻则先减小后增加,弛豫时间先增加后减小,弛豫时间分布系数无明显变化趋势。由此可以推断:(1)白皮松针叶在各浓度Zn2+胁迫7d后只受到轻微的伤害或者说还没受害;14d后时各浓度Zn2+胁迫对白皮松针叶均有明显伤害,且此时可能是受害最严重时期;21d后低浓度Zn2+胁迫对白皮松针叶已经不起作用,而高浓度继续受害,这可能是由于针叶细胞内产生某种抗性机制所致。(2)白皮松针叶在Zn2+浓度小于2000 mg·L-1时,前期有受害现象,但14d以后白皮松针叶通过自身调节开始适应,也就是说白皮松可以忍耐2000 mg·L-1以下Zn2+胁迫,当Zn2+浓度大于2000 mg·L-1时,各参数相比对照变化明显,说明白皮松针叶不能忍耐2000 mg·L-1以上Zn2+浓度胁迫。
刘晓红等研究不同浓度的重金属Cu2+、Zn2+、Pb2+、Ni2+和Cr3+胁迫对小麦叶片的影响,结果表明,随浓度的增加胞外电阻和弛豫时间均先增加后减小,胞内电阻和弛豫时间分布系数减小[14]。这与本研究结果不完全相同,可能是木本植物与草本植物生理结构不同所致,也可能因为重金属处理时间和浓度上的不同所致,且REPO等研究发现[12-13,15],胞内电阻与细胞的大小、细胞质基质的浓度有关,当逆境引起共质体离子迁移率减小时,胞内电阻增大。胞外电阻同样依赖于细胞生理状态的变化。驰豫时间的大小反映了细胞膜组成的变化、细胞内离质体和共质体中离子的迁移率及它们对频率变化的响应,从分子水平上反映了细胞膜脂肪酸的过氧化程度;叶肉细胞的大小和质体小球的数量对驰豫时间也会产生影响。叶肉细胞中细胞质的体积以及叶绿体的大小引起细胞各向异性,对驰豫时间的分布系数产生影响。由于在试验中采用了分布电路对参数进行拟合,因此,各个参数变化的生理意义还不明确[16]。当受到O3胁迫后,垂枝桦(Betula pendula)叶片的胞外电阻和弛豫时间减小,在受到CO2胁迫后,叶片的胞内电阻增加[15],这种变化趋势与本课题组在Zn2+胁迫下得到的白皮松针叶胞内电阻率和弛豫时间的总变化趋势很相似。由上所述,可初步推测重金属Zn2+胁迫影响电阻抗参数变化可能的原因是:(1)白皮松是6a生的木本植物,白皮松根系吸收重金属离子到运输至叶,到使针叶受害需要一定时间,所以处理7 d针叶各电阻抗参数变化不大;(2)过量的Zn2+离子使细胞膜结构破坏,膜透性增加,内含物外渗尤其是离子大量外渗,使胞外电阻和胞内电阻增加。当然这种解释还有待进一步研究。
植物细胞在受到逆境因子胁迫时及之后,其结构发生改变,用电阻抗图谱能够测定出这些变化。由于植物样本的横切面面积及长度的大小会成比例地分别降低和提高阻抗,所以需要考虑组织的几何形状,一般将植物器官切取长15 mm的样本进行测定。为了消除细胞内含物等的渗出对测定结果的影响,研究人员通常从抽样至测定过程中,将植物样本在隔离的冷藏容器用塑料袋包装,并于24 h内运输,如植株没脱水则影响不大[17]。在测定过程中随测定随从冷藏容器中取样,从而降低了脱水、内含物渗出的危害[18],使取样对测定结果的影响降至最小。本研究中,重金属离子Zn2+胁迫对白皮松电阻抗参数的影响随胁迫时间和Zn2+浓度的变化而改变,表明电阻抗技术可以用于监测和评价重金属离子胁迫对木本植物的伤害。
参考文献:
[1]郭笃发.环境中铅和镉对人和动物的毒性研究[J].环境科学进展,1994,2(3):71-76.
[2]张玉秀,柴团耀.植物耐重金属机理研究进展[J].植物学报,1999,41(5):453-457.
[3]金彩霞,周启星,孙瑞莲,等.Cd、豆磺隆胁迫下黑土-小麦系统中酶活性的动态变化[J].环境科学学报,2006,26(4):632-639.
[4]张树清,张夫道,刘秀梅,等.重金属元素Cu、Zn对大白菜幼苗的毒性效应[J].农业环境科学学报,2005,24(5):838-842.
[5]ACKMANN JJ,SEITZ MA.Methods of complex impedance measurements in biological tissue[J].CRC Critical Review in Biomedical Engineering,1984,11:281-311.
[6]MACDOUGALL RC,THOMPSON RG,PIENE H.Stem electrical capacitance and resistance measurements as related to total foliar biomass of balsam fir trees[J].Canadian Journal of Forest Research,1987,17:1071-1074.
[7]GREENHAM CG,HELMS K,MULLER WJ.Influence of virus infections on impedance parameters[J].Journal of Experimental Botany,1978,29:867-877.
[8]COX MA,ZHANG MIN,WILLISON JHM.Apple bruise assessment through electrical impedance measurements[J].Journal of Horticulrural Science,1993,68:393-398.
[9]ZHANG G,RYYPPÖ A,REPO T.The electrical impedance spectroscopy of Scots pine needles during cold acclimation[J].Physiologia Plantarum,2002,115:385-392.
[10]ZHANG G,RYYPPÖ A,VAPAAVUORI E,et al.Quantification of additive response and stationarity of frost hardiness by photoperiod and temperature in Scots pine[J].Canadian Journal of Forest Research,2003,33:1772-1784.
[11]CAPPIELLO P E,DUNHAM S W.Seasonal variation in low-temperature tolerance of Vaccinium angustifolium Ait.[J].HortScience,1994,29,302-304.
[12]REPO T,ZHANG MIN,PYYPPÖ A,et al.Effects of freeze thaw injury on parameters of distributed electrical circuits of stems and needles of Scots pine seedlings at different stages of acclimation[J].Journal of Experimental Botany,1994,45:823-833.
[13]REPO T,ZHANG G,RYYPPÖ A,et al.The electrical impedance spectroscopy of Scots pine (Pinus sylvestris L.)shoots in relation to cold acclimation[J].Journal of Experimental Botany,2000,51:2095-2107.
[14]刘晓红,王国栋,张 钢.外源重金属胁迫对小麦叶片电阻抗参数的影响[J].农业环境科学学报,2007,26(6):2014-2020.
[15]REPO T,OKSANEN E,VAPAAVUORI E.Effects of elevated concentrations of ozone and carbon dioxide on the electrical impedance of leaves of silver birch(Betula pendula)clones[J].Tree Physiology,2004,24:833-843.
[16]张 钢,肖建忠,陈段芬.测定植物抗寒性的电阻抗图谱法[J].植物生理与分子生物学报,2005,31(1):19-26.
[17]DEHAYES DH,WAITE CE,INGLE MA.Storage temperature and duration influence cold tolerance of red spruce foliage[J].Forest Science,1990,36:1153-1158.
[18]BURR KE,TINUS RW,WALLNER SJ,et al.Comparison of three cold hardiness tests for conifer seedlings[J].Tree Physiology,1990,6:351-369.
Influence of Zn2+Stress on Electrical Impedance Spectroscopy Parameters of Pinus bungeana Needles
Abstract:To study membrane electrical properties of Pinus bungeana needles under heavy metalion Zn2+stress,potted seedlings of 6-year-old Pinus bungeana were measured the electrical impedance spectroscopy.The extracellular resistance,intracellular resistance,relaxation time,distribution coefficient of relaxation time,high-frequency resistance and low-frequency resistance of Pinus bungeana needles were determined under Zn2+stress (200,500,1000,2000,3000 mg·L-1and 0 mg·L-1as the control,respectively).The results showed that under different concentrations of Zn2+stress,with the increase in treatment time,the extracellular resistance and low frequency resistance increased,the intracellular resistance and high-frequency resistance decreased first and then increased,the relaxation time first increased and then decreased,whereas the distribution coefficient of relaxation time had no obvious change.In various concentrations of Zn2+stress,with the increase of the Zn2+concentrations,there was no obvious change in each parameter 7 days after treatment.However,14 days after treatment all parameters increased with the increase in Zn2+concentration compared with the control,and the extracellular resistance and low resistance increased by 115%-235%,and intracellular resistance increased by 34%-95%.21 days After treatment,except for the distribution coefficient of relaxation time,all the other parameters in Zn2+concentration of 3000 mg·L-1differed significantly to the control,and the extracellular resistance and low resistance increased by 129%,intracellular resistance increased by 232%,relaxation time reduced by 74%,and high-frequency resistance increased by 216%.28 days after treatment,the extracellular resistance,intracellular resistance,high-frequency resistance and low frequency resistance had significant differences from the control under Zn2+stress in concentrations of 200,2000 and 3000 mg·L-1,respectively.In conclusion,the Zn2+treatment had significant damages to Pinus bungeana needles 14 days later,suggesting when might be the most sensitive period to Zn2+stress.Pinus bungeana needles could not tolerate the Zn2+stress over concentration of 2000 mg L-1.
Key words:electrical impedance parameter;membrane;heavy metalion;Pinus bungeana
中图分类号:S687.2
文献标识码:A
文章编号:1000-1700(2010)06-0667-06
收稿日期:2010-07-10
基金项目:河北农业大学留学回国人员启动基金项目(200406)

