白皮松天然群体遗传多样性的EST-SSR分析
【类型】期刊
【作者】赵罕,郑勇奇,李斌,张川红,林富荣,于雪丹,程蓓蓓,黄平(中国林业科学研究院林业研究所林木遗传育种国家重点实验室国家林业局林木培育重点实验室;中国林业科学研究院经济林研究开发中心)
【作者单位】中国林业科学研究院林业研究所,林木遗传育种国家重点实验室,国家林业局林木培育重点实验室;中国林业科学研究院经济林研究开发中心
【刊名】林业科学研究
【关键词】 白皮松;天然群体;EST-SSR;遗传多样性
【资助项】国家科技支撑计划课题(2013bad01b06)
【ISSN号】1001-1498
【页码】P474-480
【年份】2019
【期号】第4期
【期刊卷】1;|7;|8;|5;|2
【摘要】为探讨白皮松群体间遗传变异规律,使用7对EST-SSR引物对分布区内21个白皮松天然群体的遗传多样性及遗传分化水平进行了研究。结果表明:7对引物在21个白皮松天然群体的663个单株中共检测到14个多态性位点。各群体间有效等位基因数(Ne)、Shannon’s信息指数(I)、观测杂合度(Ho)、期望杂合度(He)、Nei’s期望杂合度(Nei’s)分别为1.156 5 1.601 9、0.133 5 0.492 5、0.138 4 0.397 3、0.0860 0.342 8、0.084 6 0.337 4。白皮松群体间遗传分化系数(Fst)平均为0.215 2,基因流(Nm)值平均为0.911 9,群体间基因交流总体较少,遗传分化较大。白皮松多样性水平在分布区内呈规律性变化,多样性分布的中心区域主要在西部、南部,具有从西向东,从南向北依次减少的趋势。
【全文】 文献传递
白皮松天然群体遗传多样性的EST-SSR分析
摘要:为探讨白皮松群体间遗传变异规律,使用7对EST-SSR引物对分布区内21个白皮松天然群体的遗传多样性及遗传分化水平进行了研究。结果表明:7对引物在21个白皮松天然群体的663个单株中共检测到14个多态性位点。各群体间有效等位基因数(Ne)、Shannon’s 信息指数(I)、观测杂合度(Ho)、期望杂合度(He)、Nei’s期望杂合度(Nei’s)分别为1.156 5![]() 1.601 9、0.133 5
1.601 9、0.133 5![]() 0.492 5、0.138 4
0.492 5、0.138 4![]() 0.397 3、0.0860
0.397 3、0.0860![]() 0.342 8、0.084 6
0.342 8、0.084 6![]() 0.337 4。白皮松群体间遗传分化系数(Fst)平均为0.215 2,基因流(Nm)值平均为0.911 9,群体间基因交流总体较少,遗传分化较大。白皮松多样性水平在分布区内呈规律性变化,多样性分布的中心区域主要在西部、南部,具有从西向东,从南向北依次减少的趋势。
0.337 4。白皮松群体间遗传分化系数(Fst)平均为0.215 2,基因流(Nm)值平均为0.911 9,群体间基因交流总体较少,遗传分化较大。白皮松多样性水平在分布区内呈规律性变化,多样性分布的中心区域主要在西部、南部,具有从西向东,从南向北依次减少的趋势。
关键词:白皮松;天然群体;EST-SSR;遗传多样性
白皮松(Pinus bungeana Zucc.)是我国特有的乡土树种,在我国栽培历史悠久[1],古代多植于皇家园林、陵寝以及寺庙等处。现在,白皮松不但是我国重要的针叶绿化树种,而且在木材、药用、食用方面均具有重要开发利用价值,是我国北方和西部地区园林绿化与生态工程造林的重要树种;同时世界各地也广泛引种,[2-3]。白皮松天然分布以山体走向为依托,主要分布在太行山、吕梁山、中条山、秦岭及大巴山区。由于环境条件的破坏,人为干扰及白皮松自身更新困难等因素,白皮松天然群体目前大多退化至山顶或山崖附近,数量较少,地理隔离现象较为普遍,多样性保存面临较大挑战。由于白皮松生长缓慢,通过长期进化所形成的种内变异来之不易;因此,对白皮松遗传资源进行合理有效的保护具有重要的意义。
了解物种的分布规律及其遗传多样性状况,是人们制定合理决策的理论基础[4]。对白皮松天然群体的表型多样性及利用同工酶的遗传多样性[5-6]的研究表明,白皮松在群体间和群体内均存在广泛的变异。与松属的其他树种相比,白皮松群体间的表型、同工酶标记所计算的遗传分化系数在松属植物中均处于较高的水平;而其群体间的平均遗传多样性水平则相对较低。在分子水平上,目前人们对白皮松所进行的研究还相对较少,仅李斌[6]使用AFLP分子标记对白皮松4个群体的多样性水平进行了研究,其他分子标记在白皮松遗传多样性中的研究还未见报道。SSR又称微卫星,是指以少数几个核苷酸为单位的串联重复序列。尽管目前存在AFLP、ISSR、SCAR、SRAP、STS等各类分子标记,SSR标记以其多态性高、共显性遗传、适合高通量分析以及DNA用量少、对DNA质量要求不高等诸多优点在植物遗传多样性研究、基因型鉴定、遗传图谱构建、QTL 定位、种质资源保存、濒危物种保护、基因流监测、基因突变检测及系统发育等领域具有广泛的应用[7-8]。本文以SSR分子标记为手段,对白皮松天然分布区内21个天然群体进行了分析,为了解不同群体及分布区内白皮松遗传多样性及分布规律提供参考。
1 试验材料和方法
1.1 试验材料
在对白皮松分布区全面了解的基础上,依山势走向对山西、河南、湖北、甘肃、陕西等地的天然林进行取样(表1)。为尽量避免采样单株之间的亲缘关系,采样时单株间至少保持10 m的距离,其中,陕西蓝田天然群体,甘肃天水A、B、C群体,甘肃两当,甘肃徽县,山西临汾A群体为课题组2000年秋季所采种子,其他试验材料为2011年秋季所采针叶。白皮松种子采摘后放入锡箔纸中以真空状态4 ℃保存;将针叶从树体取下后和硅胶一起放入自封袋中,带回试验室后-80 ℃冰箱保存。种子在提取DNA前放入纱布中,每天用清水冲洗1次,室温催芽,萌芽后利用其胚进行DNA提取。
表1 白皮松采样地点及样品信息
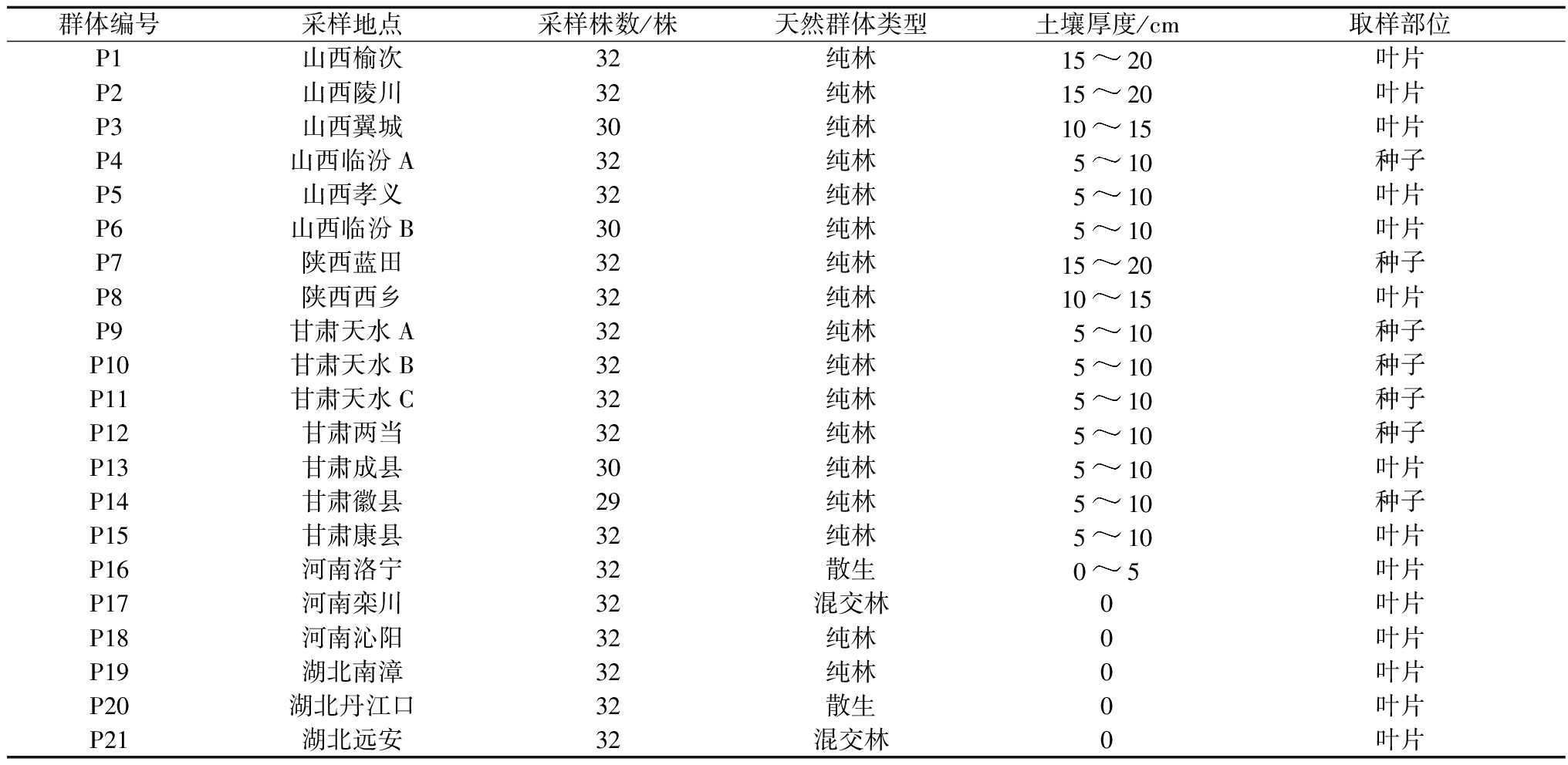
群体编号采样地点采样株数/株天然群体类型土壤厚度/cm取样部位P1山西榆次32纯林1520叶片P2山西陵川32纯林1520叶片P3山西翼城30纯林1015叶片P4山西临汾A32纯林510种子P5山西孝义32纯林510叶片P6山西临汾B30纯林510叶片P7陕西蓝田32纯林1520种子P8陕西西乡32纯林1015叶片P9甘肃天水A32纯林510种子P10甘肃天水B32纯林510种子P11甘肃天水C32纯林510种子P12甘肃两当32纯林510种子P13甘肃成县30纯林510叶片P14甘肃徽县29纯林510种子P15甘肃康县32纯林510叶片P16河南洛宁32散生05叶片P17河南栾川32混交林0叶片P18河南沁阳32纯林0叶片P19湖北南漳32纯林0叶片P20湖北丹江口32散生0叶片P21湖北远安32混交林0叶片
注:甘肃天水A、B、C群体,甘肃两当,甘肃徽县,山西临汾A群体为课题组2000年所采种子,其他试验材料为2011年所采叶片。
1.2 试验方法
1.2.1 基因组 DNA的提取 基因组DNA的提取均采用CTAB法,1%琼脂糖检测DNA质量,使用NanoDrop 2000 超微量分光光度计测定DNA的浓度和纯度,将DNA稀释到20![]() 100 ng·uL-1,放入4 ℃冰箱备用。
100 ng·uL-1,放入4 ℃冰箱备用。
1.2.2 PCR扩增 采用3 条引物来进行PCR 扩增。第1 条引物由SSR正向引物的5′端和M13相连组成(5′-TGT AAA ACG ACG GCC AGT-3′);第2 条引物为正常的SSR反向引物,第3 条引物是5′端标有CY5荧光标记的M13 尾巴引物(CY5-TGT AAA ACG ACG GCC AGT)。PCR反应体系共10 μL,其中,2×Taq PCR MasterMix 5 μL,正反向引物各0.2 μL(浓度10 μmol·L),CY5荧光引物0.2 μL(浓度10 μmol·L),DNA0.4 μL,水4 μL。反应程序分2步,第1步:95 ℃预变性5 min;95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸45 s,30个循环;第2步:95 ℃变性30 s,53 ℃退火30 s,72 ℃延伸45 s,8个循环;72 ℃延伸10 min。
1.2.3 毛细管电泳 将甲酰胺与分子量内标按100∶1的体积比混匀后,取15 μL加入上样板中,再加入0.4 μL PCR产物,然后使用BECKMAN CEQ8000遗传分析仪对PCR结果进行毛细管电泳。
1.2.4 数据分析 每对引物作为一对等位基因位点,将基因型按照AA、AB、BB的格式进行统计。使用POPGENE32软件计算群体有效等位基因数(Ne)、Shannon’s信息指数(I)、期望杂合度(Ho)、观测杂合度(He)、Nei’s期望杂合度(Nei’s)、固定指数(Fis)、F统计量(Fst)、基因流(Nm)、遗传距离和遗传一致度;并以χ2方检验检测群体的Hardy-Weinberg平衡。根据遗传相似度与遗传距离,以UPGMA方法,利用软件NTSYS-pc2.1绘制各群体聚类分析图。
2 结果与分析
2.1 引物筛选
从已发表的309对松属SSR引物中,筛选出了86对扩增效果较好的引物。扩增结果表明:7对引物具有多态性(表2)。图1为Y3引物的扩增结果。
表2 引物编号及序列
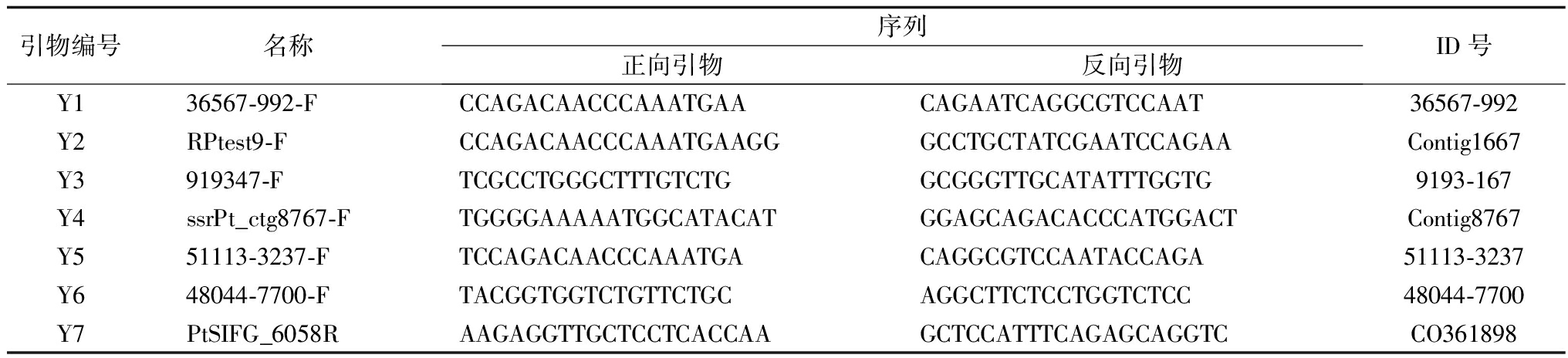
引物编号名称序列正向引物反向引物ID号Y136567⁃992⁃FCCAGACAACCCAAATGAACAGAATCAGGCGTCCAAT36567⁃992Y2RPtest9⁃FCCAGACAACCCAAATGAAGGGCCTGCTATCGAATCCAGAAContig1667Y3919347⁃FTCGCCTGGGCTTTGTCTGGCGGGTTGCATATTTGGTG9193⁃167Y4ssrPt_ctg8767⁃FTGGGGAAAAATGGCATACATGGAGCAGACACCCATGGACTContig8767Y551113⁃3237⁃FTCCAGACAACCCAAATGACAGGCGTCCAATACCAGA51113⁃3237Y648044⁃7700⁃FTACGGTGGTCTGTTCTGCAGGCTTCTCCTGGTCTCC48044⁃7700Y7PtSIFG_6058RAAGAGGTTGCTCCTCACCAAGCTCCATTTCAGAGCAGGTCCO361898
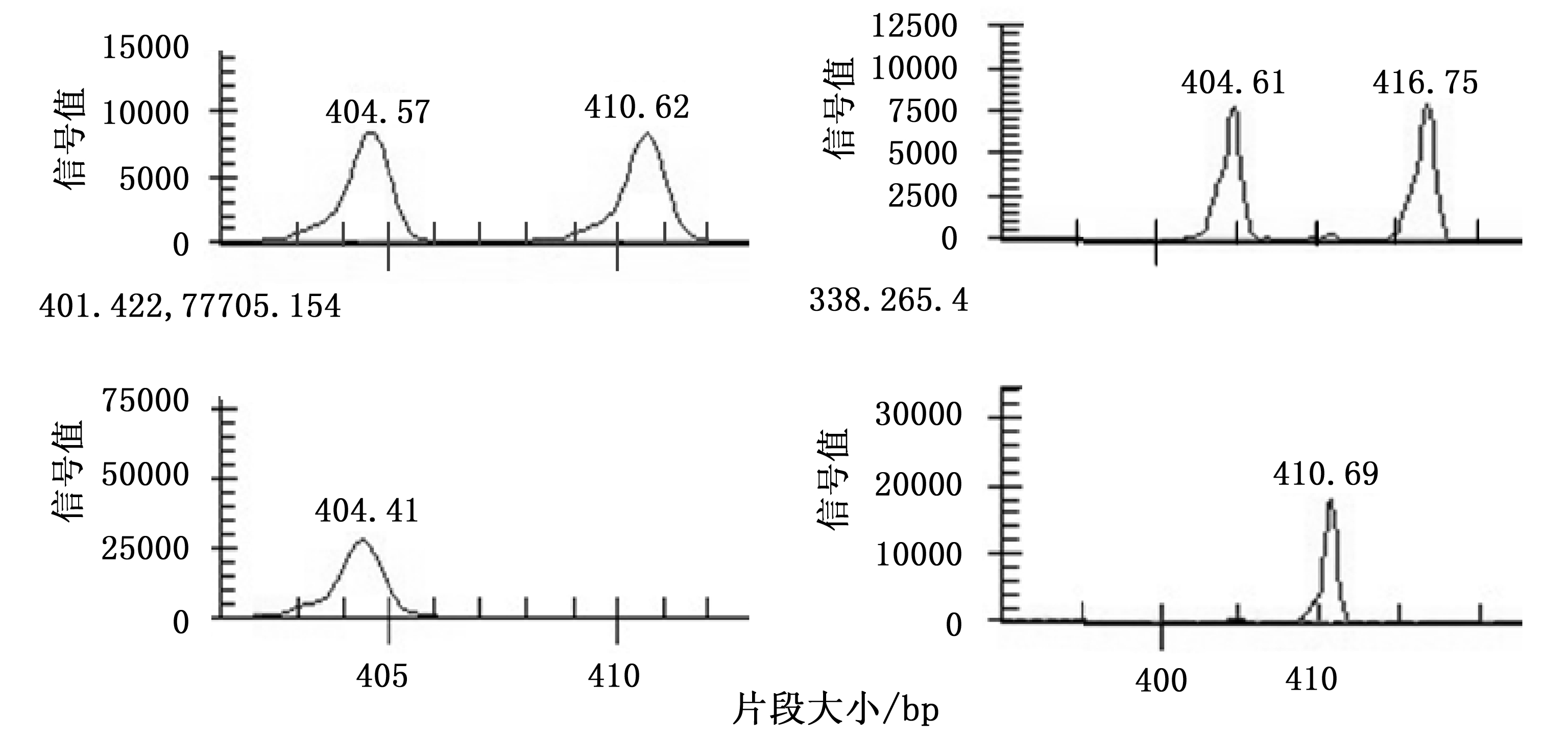
图1 引物Y3在甘肃成县群体的扩增结果
2.2 白皮松天然群体的遗传多样性
在21个白皮松天然群体的663个单株中,7对EST-SSR引物共检测到14个多态性位点。各位点有效等位基因数(Ne)、Shannon’s 信息指数 (I)、观测杂合度(Ho)、期望杂合度(He)、Nei’s期望杂合度分别为1.021 3![]() 1.662 0、0.058 6
1.662 0、0.058 6![]() 0.587 7、0.015 1
0.587 7、0.015 1![]() 0.543 0、0.020 9
0.543 0、0.020 9![]() 0.398 6、0.020 9
0.398 6、0.020 9![]() 0.398 3;平均值分别为1.362 2、0.401 0、0.221 5、0.249 1、0.248 9(表3)。
0.398 3;平均值分别为1.362 2、0.401 0、0.221 5、0.249 1、0.248 9(表3)。
表3 白皮松天然群体位点间遗传多样性统计
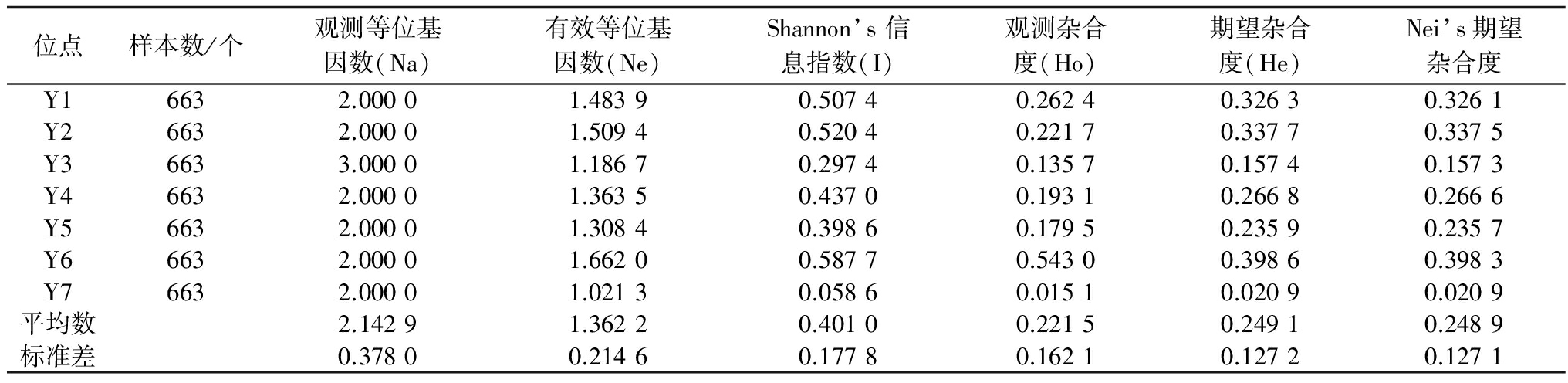
位点样本数/个观测等位基因数(Na)有效等位基因数(Ne)Shannon’s信息指数(I)观测杂合度(Ho)期望杂合度(He)Nei’s期望杂合度Y16632.00001.48390.50740.26240.32630.3261Y26632.00001.50940.52040.22170.33770.3375Y36633.00001.18670.29740.13570.15740.1573Y46632.00001.36350.43700.19310.26680.2666Y56632.00001.30840.39860.17950.23590.2357Y66632.00001.66200.58770.54300.39860.3983Y76632.00001.02130.05860.01510.02090.0209平均数2.14291.36220.40100.22150.24910.2489标准差0.37800.21460.17780.16210.12720.1271
从表4看出:各群体间有效等位基因数(Ne),Shannon’s 信息指数(I),观测杂合度(Ho),期望杂合度(He),Nei’s期望杂合度分别为1.156 5![]() 1.601 9,0.133 5
1.601 9,0.133 5![]() 0.492 5,0.138 4
0.492 5,0.138 4![]() 0.397 3,0.086
0.397 3,0.086![]() 0.342 8,0.084 6
0.342 8,0.084 6![]() 0.337 4;平均值分别为1.309 7,0.312 7,0.221 4,0.199 4,0.196 3。
0.337 4;平均值分别为1.309 7,0.312 7,0.221 4,0.199 4,0.196 3。
各群体按照多样性参数排序(表4)结果表明:各群体多样性排序在不同的参数中虽然有所出入,但基本相同。位于白皮松自然分布区域西南和东南边界的康县和远安县多样性水平最高,秦岭西南侧和大巴山区群体的白皮松多样性水平也相对较高,秦岭东侧的洛宁、栾川、沁阳及中条山区、太行山区、吕梁山区的白皮松群体多样性水平相对较低。从各群体的地理分布与多样性参数的对比可以看出:在白皮松自然分布区内,其多样性水平呈规律性的变化,多样性水平具有从南向北、从西向东逐渐降低的趋势。
表4 白皮松天然群体遗传多样性及排序(从小到大)
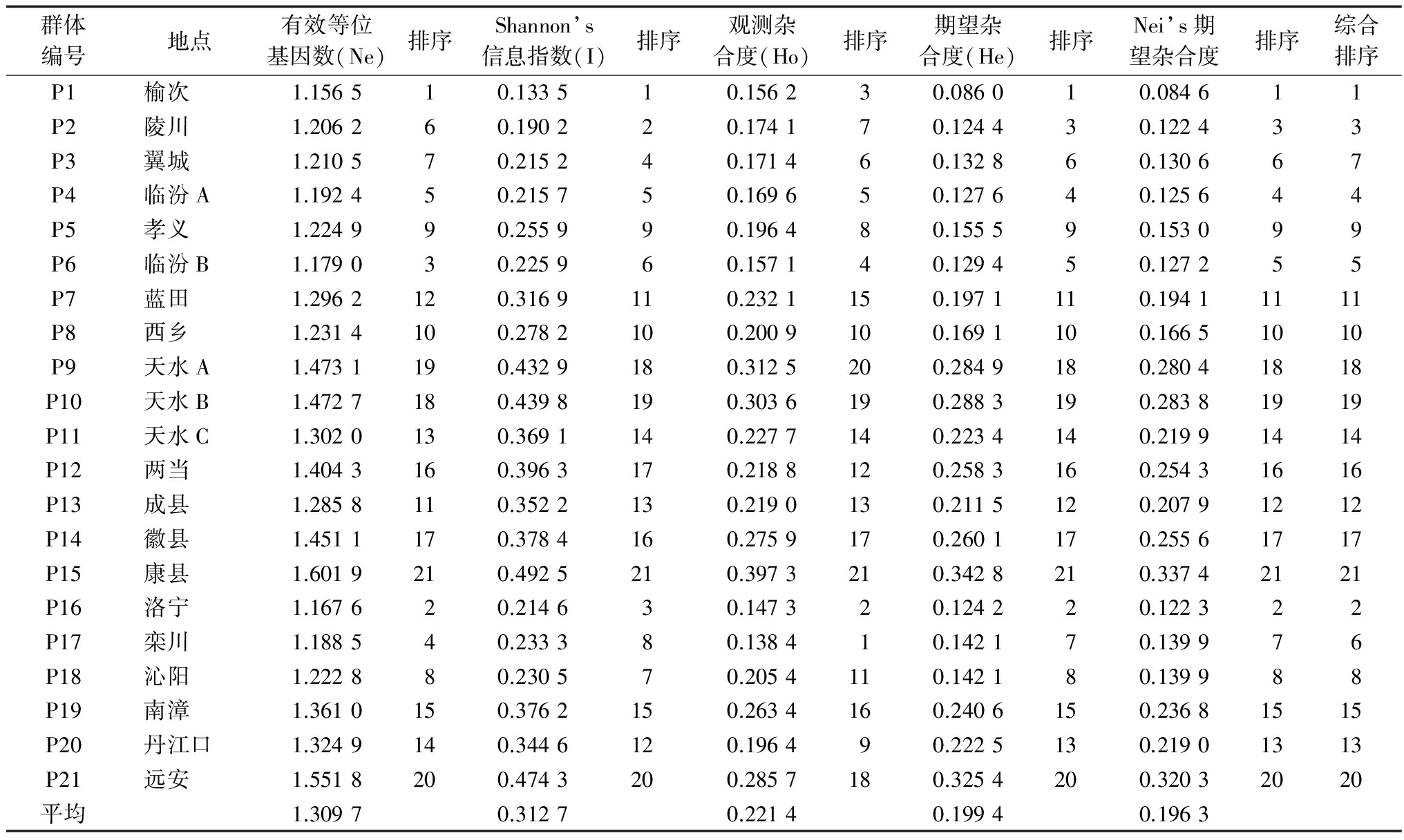
群体编号地点有效等位基因数(Ne)排序Shannon’s信息指数(I)排序观测杂合度(Ho)排序期望杂合度(He)排序Nei’s期望杂合度排序综合排序P1榆次1.156510.133510.156230.086010.084611P2陵川1.206260.190220.174170.124430.122433P3翼城1.210570.215240.171460.132860.130667P4临汾A1.192450.215750.169650.127640.125644P5孝义1.224990.255990.196480.155590.153099P6临汾B1.179030.225960.157140.129450.127255P7蓝田1.2962120.3169110.2321150.1971110.19411111P8西乡1.2314100.2782100.2009100.1691100.16651010P9天水A1.4731190.4329180.3125200.2849180.28041818P10天水B1.4727180.4398190.3036190.2883190.28381919P11天水C1.3020130.3691140.2277140.2234140.21991414P12两当1.4043160.3963170.2188120.2583160.25431616P13成县1.2858110.3522130.2190130.2115120.20791212P14徽县1.4511170.3784160.2759170.2601170.25561717P15康县1.6019210.4925210.3973210.3428210.33742121P16洛宁1.167620.214630.147320.124220.122322P17栾川1.188540.233380.138410.142170.139976P18沁阳1.222880.230570.2054110.142180.139988P19南漳1.3610150.3762150.2634160.2406150.23681515P20丹江口1.3249140.3446120.196490.2225130.21901313P21远安1.5518200.4743200.2857180.3254200.32032020平均1.30970.31270.22140.19940.1963
2.3 白皮松天然群体间遗传分化
白皮松群体间的遗传分化系数(Fst)与基因流(Nm)的变动范围分别为: 0.080 1![]() 0.336 4与0.493 1
0.336 4与0.493 1![]() 2.870 0;平均值分别为0.215 2与0.911 9(表5),说明白皮松群体间具有较大的遗传分化和相对较小的基因流。相关分析表明:21个群体间的遗传相似系数为0.616 8
2.870 0;平均值分别为0.215 2与0.911 9(表5),说明白皮松群体间具有较大的遗传分化和相对较小的基因流。相关分析表明:21个群体间的遗传相似系数为0.616 8![]() 0.999 5。根据群体间的遗传相似性系数,按UPGMA法对各个白皮松群体进行聚类分析并作聚类图,在遗传距离为0.05处将白皮松分为4个类群(图2),其中,P13(甘肃成县)群体为第1个类群,这个群体与其他群体遗传距离相对较大,在遗传距离0.33处与其他群体分开。P14(甘肃徽县)群体为第2个类群,该类群在遗传距离为0.17处与其他群体分开;P9(甘肃天水A)、P10(甘肃天水B)、P12(甘肃两当)、P15(甘肃康县)、P21(湖北远安)为第3个类群;其他群体为第4个类群。除P21群体外,前3类中其他群体均分布在秦岭西段山区,这说明这一区域是白皮松分化较大的区域;而其他群体分化水平则相对较低,其中山西的太行山、吕梁山、中条山各群体均被聚为一个小的类别,说明这一区域遗传结构较为相似。
0.999 5。根据群体间的遗传相似性系数,按UPGMA法对各个白皮松群体进行聚类分析并作聚类图,在遗传距离为0.05处将白皮松分为4个类群(图2),其中,P13(甘肃成县)群体为第1个类群,这个群体与其他群体遗传距离相对较大,在遗传距离0.33处与其他群体分开。P14(甘肃徽县)群体为第2个类群,该类群在遗传距离为0.17处与其他群体分开;P9(甘肃天水A)、P10(甘肃天水B)、P12(甘肃两当)、P15(甘肃康县)、P21(湖北远安)为第3个类群;其他群体为第4个类群。除P21群体外,前3类中其他群体均分布在秦岭西段山区,这说明这一区域是白皮松分化较大的区域;而其他群体分化水平则相对较低,其中山西的太行山、吕梁山、中条山各群体均被聚为一个小的类别,说明这一区域遗传结构较为相似。
表5 白皮松天然群体遗传分化系数及基因流
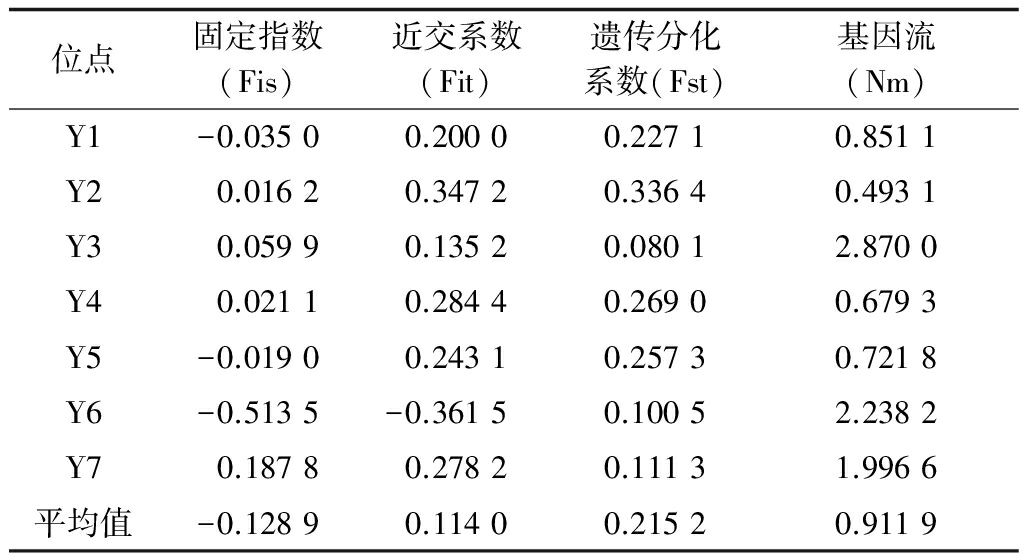
位点固定指数(Fis)近交系数(Fit)遗传分化系数(Fst)基因流(Nm)Y1-0.03500.20000.22710.8511Y20.01620.34720.33640.4931Y30.05990.13520.08012.8700Y40.02110.28440.26900.6793Y5-0.01900.24310.25730.7218Y6-0.5135-0.36150.10052.2382Y70.18780.27820.11131.9966平均值-0.12890.11400.21520.9119
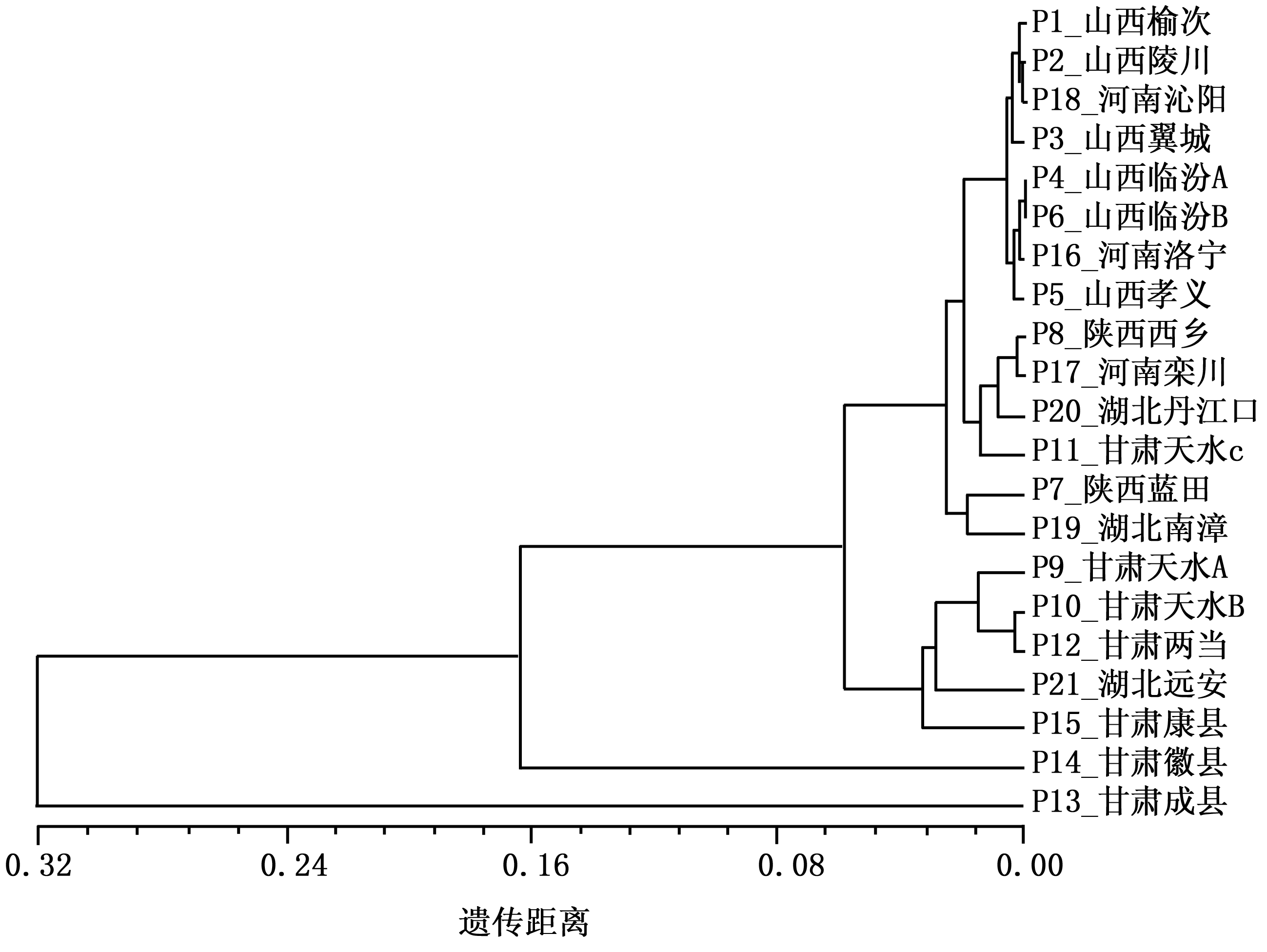
图2 白皮松天然群体聚类图(P1![]() P13为群体编号)
P13为群体编号)
3 结论与讨论
3.1 SSR分子标记的筛选
由于SSR引物具有一定的保守性和稳定性,在不同物种中具有一定的通用性,特别是亲缘关系相对较近的物种,因此,从近缘物种中筛选SSR引物也是一种较为高效的方法[9];但由于物种自身特点不同,其通用率也不相同。尹佟明等[10]对SSR引物在松树中的通用性进行了研究,结果表明,松属种间能通用且在单株树中为杂合的EST位点比例相对较低。艾畅[11]对源自辐射松、欧洲赤松、瑞士五针松、火炬松的140对SSR引物进行了种间通用性试验,结果表明,能在马尾松上扩增出条带的引物占56.43%,多态性较好的引物占5.71%。冯锦霞[12]对153对松属近缘种SSR引物进行了筛选,结果从中获得了8对多态性SSR引物,多态性比率为5.2%。本文从309对松属已发表的SSR引物中,最终筛选出了7对具有多态性位点的引物,通用率为2.27%,相对于松属其他树种的研究结果,SSR引物在白皮松中的通用性相对较小,7对最终筛选出的引物均为EST-SSR。很多研究表明,EST-SSR相关的基因可能涉及蛋白质代谢、转运、转录、发育、信号传导等功能,能够更为准确地反映出遗传信息,具有更强的基因型鉴别能力[13-15]。
3.2 白皮松群体的遗传多样性
相对于同工酶和AFLP标记对白皮松的研究结果,SSR标记遗传多样性指数大于同工酶标记(He=0.098 6),与AFLP(Shannon’s信息指数I=0.283![]() 0.437)相似。群体遗传分化与同工酶相似(Gst=0.243,Nm=0.78),大于AFLP标记(Gst=0.102)。
0.437)相似。群体遗传分化与同工酶相似(Gst=0.243,Nm=0.78),大于AFLP标记(Gst=0.102)。
在松属其他树种的SSR分析中,北美短叶松的Ne和Nei’s期望杂合度均值分别为1.187![]() 1.321和0.118
1.321和0.118![]() 0.194[16]。赤松观测杂合度和期望杂合度分别为0.185、0.508[17]。火炬松观测和期望杂合度分别介于0.482
0.194[16]。赤松观测杂合度和期望杂合度分别为0.185、0.508[17]。火炬松观测和期望杂合度分别介于0.482![]() 0.559和0.626
0.559和0.626![]() 0.679[18]。东部白松观测和期望杂合度分别为0.567
0.679[18]。东部白松观测和期望杂合度分别为0.567![]() 0.867和0.758
0.867和0.758![]() 0.867;西部白松观测和期望杂合度分别为0.567
0.867;西部白松观测和期望杂合度分别为0.567![]() 0.867和0.774
0.867和0.774![]() 0.837[19]。油松和马尾松期望杂合度分别为0.561 2
0.837[19]。油松和马尾松期望杂合度分别为0.561 2![]() 0.742和0.478 6,观测杂合度分别为0.368 9
0.742和0.478 6,观测杂合度分别为0.368 9![]() 0.585 2和0.520 8 [20-21]。白皮松观测、期望杂合度和Nei’s期望杂合度分别为0.221 5、0.249 1、0.248 9,相对于其他松属树种,白皮松多样性处于较低水平。这可能与白皮松人为破坏严重、小群体及地理隔离等因素有关。
0.585 2和0.520 8 [20-21]。白皮松观测、期望杂合度和Nei’s期望杂合度分别为0.221 5、0.249 1、0.248 9,相对于其他松属树种,白皮松多样性处于较低水平。这可能与白皮松人为破坏严重、小群体及地理隔离等因素有关。
3.3 白皮松群体间多样性分布规律
分析表明:白皮松各群体遗传多样性表现出一定的地理规律,在秦岭西部的甘肃康县、天水、成县、徽县均表现出较高的遗传多样性,并且这一区域白皮松分布较为集中,分化较大,这可能是由于这一区域地形较为复杂,气候条件变化较大,更容易形成地理隔离及该区域所处的位置与裸子植物多样性中心重合相关[22-25]。推测这一区域可能是白皮松起源及遗传多样性的中心区域。
丹江口、南漳、远安等大巴山南部区域群体遗传多样性水平也相对较高,说明这一区域多样性也较为丰富;但是其群体规模都相对较小,片段化严重,推测其群体曾经历过较大的干扰和破坏,或者是由于气候变化的原因,这一区域的群体适应性正在逐步下降。秦岭东部区域除蓝田外,其他群体及北部的山西各群体遗传多样性均相对较低,这可能是由于白皮松在历史上的迁移是沿着从南向北、从西向东的路线进行的。
3.4 白皮松群体间基因流及遗传分化
本研究中白皮松基因流(Nm)﹤1,说明白皮松在群体间的基因交流不足,这可能与白皮松群体间地理隔离较大所导致的基因交流障碍有关。白皮松群体遗传分化系数(Fst)平均值为0.215 2(>0.15),表明白皮松在群体间具有较高的遗传分化水平。前人[26]对松柏类植物的多样性研究结果表明:裸子植物遗传分化相对较小,种内分化的平均值与中值分别为0.116和0.088。白皮松遗传分化相对较大可能与群体间隔离严重及小群体所导致的自交相关。虽然风媒传粉的树种受地理隔离的影响相对较小,但也有研究表明,隔离种群的自交率是大种群的8倍[27-28]。由于白皮松群体在各个山系中主要呈斑块状分布,并且大多数群体退缩至个别的山头,相对于大面积分布的群体可能经历了更为严峻的自然选择过程,在地形、环境及群体规模等因素的作用下,群体结构可能会出现较大的波动[29]。
在所分析的21个群体中,甘肃成县、甘肃徽县分别被单独划分为一个类别,说明这2个群体的基因频率类别相对于其他群体较为独特。由于这2个群体均处于横断山-秦岭生物多样性的中心地区,可能与这一区域丰富的遗传多样性相关。
甘肃两当、天水、康县与湖北远安被聚为一类,说明白皮松在这些群体具有相似的遗传结构,北部大部分群体与中部群体聚在一起,说明白皮松在北部区域遗传背景相对简单。
参考文献:
[1] 陆素娟,李乡旺.松属的起源、演化及扩散[J].西北林学院学报,1999,14(3):1-5
[2] 吴中伦.中国松属的分类与分布[J].植物分类学报,1956,5(3):131-163
[3] Lee K C,Ahn K Y.A Study on the diversifying of plant species for the landscape construction in Korea[J]. Seoul national university journal of agricultural sciences,1991,16(1):67-80
[4] Agarwal M,Shrivastava N,Padh H.Advances in molecular marker techniques and their applications in plant sciences[J].Plant cell Rep,2008,27(4):617-631
[5] 李 斌,顾万春,卢宝铭.白皮松天然群体种实性状表型多样性研究[J].生物多样性,2002,10(2):181-188
[6] 李 斌.白皮松遗传多样性及其核心种质保护策略研究[D].北京:北京林业大学,2002
[7] 李义良,赵奋成,张应中,等.分子标记在松树遗传与进化研究中的应用[J].分子植物育种,2009,7(5):1004-1009
[8] 程小毛,黄晓霞.SSR标记开发及其在植物中的应用[J].中国农学通报,2011,27(5):304-307
[9] Chistiakov D A,Hellemans B,Filip A M.Microsatellites and their genomic distribution, evolution,function and applications:A review with special reference to fish geneties[J].Aquaculture,2006,255:1-29
[10] 尹佟明,李 东,陈 颖,等.马尾松表达序列标签多态性初步分析[J].南京林业大学学报,2004,40(6):176-180
[11] 艾 畅.马尾松无性系种子园遗传多样性及其自由授粉子代父本组成研究[D].南京:南京林业大学,2004
[12] 冯锦霞.古巴加勒比松遗传资源研究[D].北京:中国林业科学研究院,2010
[13] 宋跃朋,江锡兵,张 曼.杨树Genomic-SSR与EST-SSR分子标记遗传差异性分析[J].北京林业大学学报,2010,32(5):1-6
[14] 吴根松,张启翔,程汉武,等.梅花EST-SSR与Genomic-SSR的比较研究[J].西北农业学报,2011,20(10):120-125
[15] 杨新泉,刘 鹏,韩宗福,等.普通小麦Genomic-SSR和EST-SSR分子标记遗传差异及其与系谱遗传距离的比较研究[J].遗传学报,2005,32(4):406-416
[16] Chiovitti S L.Evolutionary genetic studies of forest trees:Genetic structure of the boreal forest tree Pinus banksiana and the molecular phylogeny of the tropical tree family dipterocarpaceae[D].Montreal:Concordia University,Canada,2006
[17] Jacquelyn B,Marilyn C,Selvadurai D.Microsatellite analysis reveals genetically distinct populations of red ping[J].American Journal of Botany, 2005,92(5):833-841
[18] Al-Rabab’ah M A,Williams C G.Population dynamics of Pinus taeda L.based on nuclear microsatellites[J].Forest Ecology and Management,2002,163:263-271
[19] Melanie M,kabwe K.N,Paul M.Assessing genetic diversity and structure of fragmented populations of eastern white pine(Pinus Strobus) and western white pine (P.Monticola) for conservation management[J].Journal of Pant Ecology,2009,2(3):143-151
[20] 程 珵.巴山松与油松的遗传分化和地理分界研究[D].西安:西北大学,2010
[21] 王鹏良.马尾松无性系种子园多年份子代遗传多样性分析[D].南京:南京林业大学,2006
[22] 李 果,沈泽昊,应俊生,等.中国裸子植物物种丰富度空间格局与多样性中心[J].生物多样性,2009,17(3):272-278
[23] 应俊生.中国种子植物物种多样性及其分布格局[J].生物多样性:2001,9(4):393-398
[24] 李 楠.论松科植物的地理分布、起源和扩散[J].植物分类学报,1995,33(2):105-130
[25] 李锡文.中国种子植物区系统计分析[J].云南植物研究,1996,18(4):363-384
[26] Petit R J,Duminil J,Fineschi S,et al.Comparative organization of chloroplas,mitochondrial and nuclear diversity in plant populations[J].Molecular Ecology,2005,14:689-701
[27] Hamrick J L,Godt M J.Allozyme diversity in plant species [M]//Brown A D H,Cless M T,Kahler A L,et al.Plant Population Genetics,Breeding,and Genetic Resources[M].Sunderland:Sinauer,1989:43-63
[28] Robledo-Arnuncio J J,Gil L.Patterns of pollen dispersal in a small population of Pinus sylvestris L.Revealed by total-exclusion paternity analysis[J].Heredity,2005,94(1):13-22
[29] Vucetich J A,WaiteT A.Spatial patterns of demography and genetic processes across the species range:null hypotheses for landscape conservation genetics[J].Conserv Genet,2003,4:639-645
Genetic Diversity Analysis of Pinus bungeana Natural Populations with EST-SSR Markers
Abstract:In order to explore the genetic variation among Pinus bungeana populations, their genetic diversity and differentiation level were studied in 21 natural populations by EST-SSR markers. 14 polymorphic loci were detected in 663 individuals among 21 natural populations using 7 pairs of EST-SSR primes. The effective number of alleles (Ne), Shannon’s information index (I), observed heterozygosity (Ho), expected heterozygosity (He) and Nei’s expected heterozygosity (Nei’s) were 1.156 5—1.601 9, 0.133 5—0.492 5, 0.138 4—0.397 3, 0.086—0.342 8, and 0.084 6—0.337 4 respectively. The results of genetic differentiation analysis showed that the average Fst and Nm were 0.215 2 and 0.911 9 respectively, the gene flow was less and the genetic differentiation was high among populations. Central regions of genetic diversity are mainly in west and south of the distribution and the genetic diversity in distribution changed regularly from west to east and from south to north.
Key words:Pinus bungeana;natural population;EST-SSR;genetic diversity
文章编号:1001-1498(2014)04-0474-07
收稿日期: 2012-06-05
基金项目: 国家科技支撑计划课题(2013BAD01B06)
* 通讯作者.E-mail:zhengyq@caf.ac.cn
中图分类号:S791.243
文献标识码:A

