白皮松EST-SSR序列分布特征及引物开发
【类型】期刊
【作者】李昕蔓,金卓颖,苏安然,杨林夕,苏晟,王磊,张军(河北农业大学林学院)
【作者单位】河北农业大学林学院
【刊名】林业与生态科学
【关键词】 白皮松;转录组;EST-SSR;多态性;引物开发
【资助项】河北农业大学科研发展基金计划(JY2018006)
【ISSN号】2096-4749
【页码】P266-272
【年份】2019
【期号】第3期
【期刊卷】7
【摘要】为解决白皮松分子标记资源相对匮乏的问题,对其针叶转录组测序结果进行检测分析及引物开发,结果在针叶转录组数据中共检测到精确型SSR位点3 268个以及复合型SSR位点104个,序列长度为10~27 bp的短序列(2 954,93.36%)占主导地位;SSR重复单元的重复次数在4~30次之间,重复次数为9次的重复单元数量最多,所占比例最大(684,20.93%);在所有142个重复单元中,A/T所占比例最大(1 508,46.14%),其次为AT/CA(280,8.57%)和TA/TC(245,7.50%);从所设计的1 151对引物中,随机选择60对EST-SSR引物,对来自不同地区的50株白皮松优树进行PCR扩增,有28对引物能扩增出清晰的条带,有效扩增率为46.67%,其中多态性引物2对,引物多态率为7.14%,多态性信息含量PIC分别为0.375、0.305。为了检验引物的多态性,又选择了7对已发表的对白皮松基因型具有多态性的SSR引物进行验证分析,结果发现,这7对引物均能扩增出清晰的条带,但对50株白皮松优树均无多态性,也侧面说明了白皮松基因序列的相对保守性。该研究结果为白皮松种质资源评价、分子标记辅助育种等方面的研究提供了参考。
【全文】 文献传递
白皮松EST-SSR序列分布特征及引物开发
LI Xinman,JIN Zhuoying,SU Anran,YANG Linxi ,SU Sheng,WANG Lei,ZHANG Jun.EST-SSR sequence distribution and primer development of Pinus bungeana[J]. Forestry and Ecological Sciences, 2019,34(3):266-272.
EST-SSR sequence distribution and primer development of Pinus bungeana
白皮松(Pinus bungeana Zucc.ex Endl.),别名三针松、白果松、蟠龙松、虎皮松、白骨松、蛇皮松等,是松科松属乔木,主要分布在山西、湖北、陕西、四川、河南、甘肃等地[1]。白皮松是东亚唯一的三针松,也是我国特有的珍贵稀有特色树种,同时也是松属中较为原始的一个类群[2]。白皮松为常绿喜光树种,四季青翠挺拔,葱郁可爱。其树姿优美,树皮为军绿色,斑驳奇特,在树木景观上能起到调和的作用。白皮松不但具有抗旱、抗风、抗寒、抗污染、病虫害少等一系列优良特性,而且可以生产木材、入药,也可食用,极具开发利用价值、研究价值和观赏价值,是我国重要的针叶绿化树种,同时被世界各地广泛引种[3-7]。
简单序列重复(Simple sequence repeats,SSR),是一种由1~6个核苷酸为重复单位组成的长达几十个核苷酸的串联重复序列,广泛分布于植物基因组中。SSR可以分为基因组SSR(g-SSR)和表达序列标签SSR(EST-SSR)。随着转录组测序技术的快速发展,EST-SSR因其具有开发相对容易,通用性高、共显性遗传、DNA用量少等独特的优点,已经成为分子标记开发首选的策略之一[8-14]。到目前为止,对白皮松的研究主要集中在育苗技术、生物学特性、生理特性、良种选育等方面,而在分子标记开发这方面的研究还很欠缺。虽然赵罕等人开发了部分白皮松的引物[6],但是引物数量依然很少,所以迫切需要开发出一些适用于白皮松的引物。为此,拟以白皮松针叶转录组测序结果为背景数据,对EST-SSR位点的组成、分布等基本特征进行分析,开发白皮松EST-SSR引物,以便进一步为白皮松的品种分类鉴定、种质资源的评价和利用、分子标记辅助育种等方面的研究提供参考。
1 材料与方法
1.1 试验材料
1.1.1 转录组数据来源 2018年4月26日,随机选取河北农业大学校园内的1株白皮松成年植株,取其顶端幼嫩针叶,干冰运输,送至北京组学生物科技有限公司进行转录组测序。
1.1.2 植物材料 引物验证及筛选所用的植物材料为河北省易县白皮松省级良种繁育基地资源收集圃收集的国内10个不同地点的50株白皮松实生优树。
1.2 试验方法
1.2.1 DNA的提取 提取DNA采用改良的CTAB法[15],用微量分光光度计测其浓度和纯度,检测合格后,将所有DNA稀释至50 ng/μL,统一放到-30℃的冰箱中储存备用。
1.2.2 转录组EST-SSR 位点的筛选及引物设计使用软件MISA对Unigene进行SSR位点搜索,标准按照:单核苷酸~六核苷酸最少重复次数分别为10、6、5、5、5和5次。采用 Primer 3软件按如下的原则进行SSR引物设计:(1)GC碱基含量在40%~60%之间;(2)PCR产物长度在100~300 bp之间;(3)退火温度在55~65℃之间,且上游和下游引物的退火温度之差小于5℃。在设计过程中,尽量避免出现引物二聚体、发卡结构、二级结构及错配的发生。同时,对赵罕等人筛选出来的7对适用于白皮松的引物进行了验证[3]。所有 SSR引物均由生工生物工程(上海)股份有限公司合成。
1.2.3 PCR扩增验证与引物筛选 20 μL的 PCR 反应体系包括:50 ng/μL的DNA模板2 μL,rTaq 聚合酶 0.5 μL,2.5 mmol/μL的dNTP 2 μL,10×buffer 2 μL,10 μM的上、下游引物各0.5 μL,ddH2O 12.5 μL。PCR 反应程序为:95 ℃ 预变性 5 min(1个循环);95 ℃ 变性 30 s,50~60 ℃ 退火30 s,72 ℃ 延伸45 s(35个循环);72 ℃ 延伸 7 min(1个循环)。PCR产物用8% 非变性聚丙烯酰胺凝胶进行检测,在270 V电压下电泳30 min,然后用硝酸银溶液染色,氢氧化钠溶液显色,最后拍照,读带。
1.3 统计与分析方法
利用Excel对所有基因序列的SSR位点数、类型及分布特征进行统计分析。对聚丙烯酰胺凝胶的结果进行分析,根据条带的有无进行数据统计,利用PIC Calc 0.6 软件计算各引物的PIC(多态性信息含量)值[16]。
2 结果与分析
2.1 白皮松转录组SSR检测结果
关于白皮松EST-SSR引物检测结果及转录组SSR重复类型分布特征的分析见表1和表2。
表1 EST-SSR引物检测结果
Table 1 Detection result of EST-SSR primer
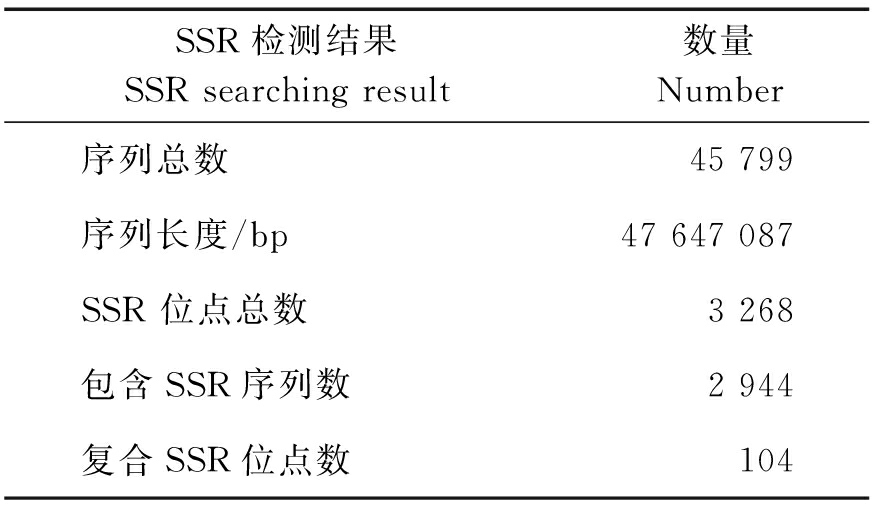
SSR检测结果SSR searching result数量Number序列总数45 799序列长度/bp47 647 087SSR 位点总数3 268 包含SSR序列数2 944复合SSR位点数104
表2 白皮松转录组SSR重复类型分布特征
Table 2 Distribution characteristics of SSR repeats inPinus bungeana transcriptome
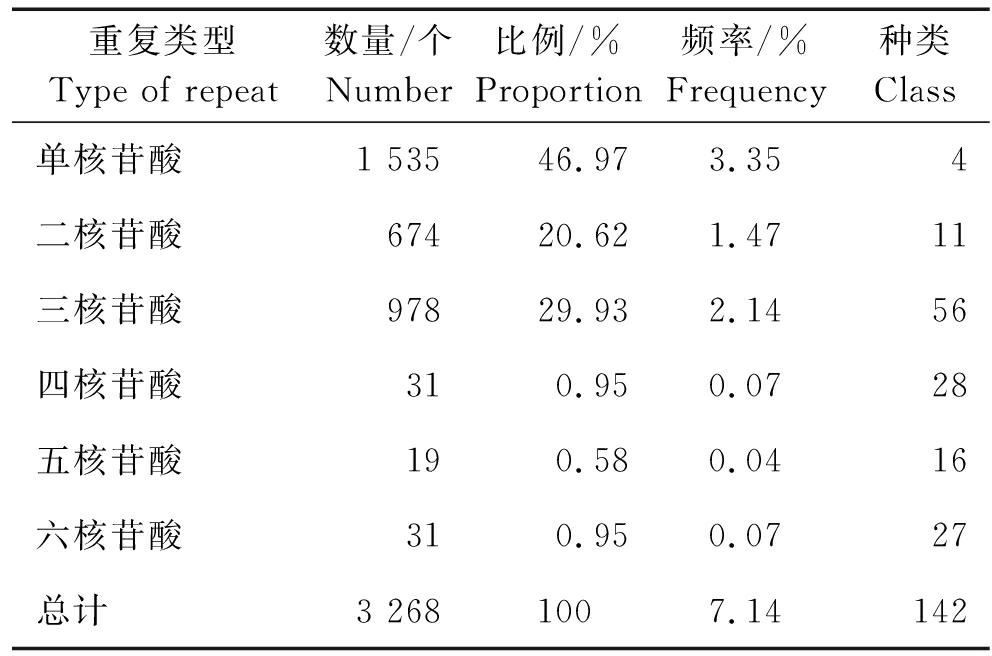
重复类型Type of repeat数量/个Number比例/%Proportion频率/%Frequency种类Class单核苷酸1 53546.973.354二核苷酸67420.621.4711三核苷酸97829.932.1456四核苷酸310.950.0728五核苷酸190.580.0416六核苷酸310.950.0727总计3 268100 7.14142
由表1、表2可知,在组装后得到的45 799 条 Unigenes序列中,其序列总长度为47 647 087 bp。共检测到SSR位点总数3 268个,其发生频率为7.14%。复合型SSR位点104个,其发生频率为0.23%。白皮松针叶转录组中SSR重复类型的种类比较丰富,其中包括单核苷酸~六核苷酸,但是各重复类型在数量上有较大差异。其中,单核苷酸重复数量最多,占到了SSR位点总数的46.97%,其出现频率为3.35%。其次是三核苷酸重复和二核苷酸重复,占到了SSR位点总数的29.93%和20.62%这3种重复类型的总数占SSR总量的97.52%。四核苷酸、五核苷酸、六核苷酸所占比例相对较小,分别占到了SSR位点总数的0.95%、0.58%、0.95%。这3种重复类型的数量之和只占到了全部精确型SSR位点的2.48%。说明白皮松EST-SSR的重复单元主要以单碱基、三碱基、二碱基为主。在白皮松针叶转录组中,一共存在142种重复单元,重复单元的种类相对较多。根据重复单元种类的多少,从多到少依次为三核苷酸(56种)、四核苷酸(28种)、六核苷酸(27种)、五核苷酸(16种)、二核苷酸(11种)、单核苷酸(4种)。
对白皮松转录组SSR基序分布特征的分析见表3。
表3 白皮松转录组SSR基序分布特征
Table 3 Distribution characteristics of SSR motifs in Pinus bungeana transcriptome
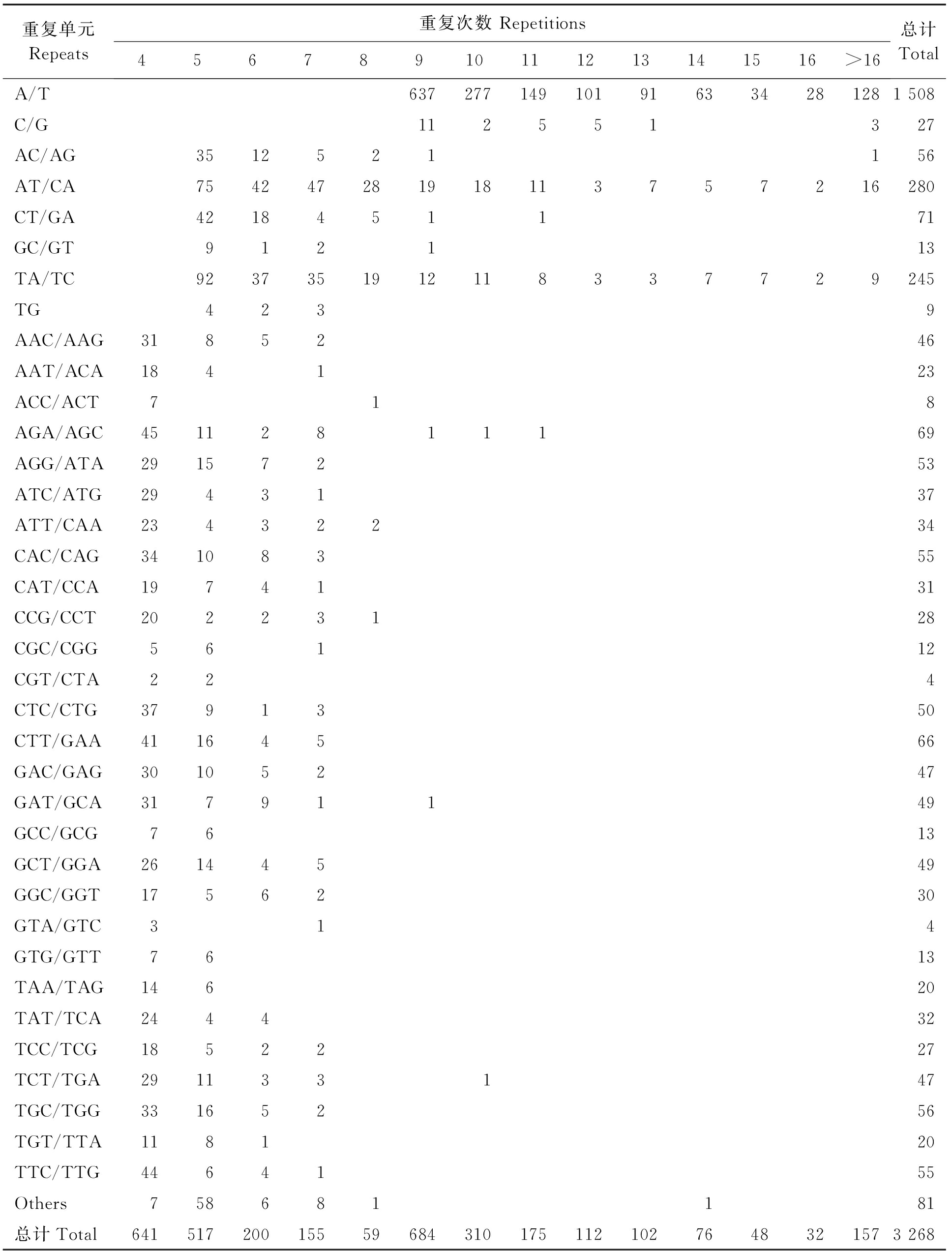
重复单元Repeats重复次数 Repetitions45678910111213141516>16总计TotalA/T637277149101916334281281 508C/G112551327AC/AG3512521156AT/CA754247281918113757216280CT/GA4218451171GC/GT912113TA/TC9237351912118337729245TG4239AAC/AAG3185246AAT/ACA184123ACC/ACT718AGA/AGC45112811169AGG/ATA29157253ATC/ATG2943137ATT/CAA23432234CAC/CAG34108355CAT/CCA1974131CCG/CCT20223128CGC/CGG56112CGT/CTA224CTC/CTG3791350CTT/GAA41164566GAC/GAG30105247GAT/GCA31791149GCC/GCG7613GCT/GGA26144549GGC/GGT1756230GTA/GTC314GTG/GTT7613TAA/TAG14620TAT/TCA244432TCC/TCG1852227TCT/TGA291133147TGC/TGG33165256TGT/TTA118120TTC/TTG4464155Others758681181总计Total641517200155596843101751121027648321573 268
由表3可知,在所有142个重复单元中,A/T所占比例最大,其数量和比例分别为1 508和46.14%。其次为AT/CA(280,8.57%),然后是TA/TC(245,7.50%)。在白皮松三核苷酸重复单元中,AGA/AGC数量最多,为69个,占全部三核苷酸SSR位点总数的7.06%。四核苷酸、五核苷酸、六核苷酸重复单元的种类相对较多,但是每个重复单元的数量相对较少。白皮松转录组的SSR重复单元的重复次数在4~30次之间,从各个重复单元的重复次数来看,重复9次的重复单元(684)最多,占到了SSR位点总数的20.93%,其发生频率为1.49%。其次是重复次数为4次和5次的重复单元,其数量分别为641个和517个,占所有SSR位点数的比例分别为19.61%和15.82%,其发生频率分别为1.40%和1.13%。
对白皮松转录组SSR位点长度分布特征的分析见表4。
由表4可知,在白皮松针叶转录组中,去除复合型SSR位点104个,剩余3 164个SSR位点,对这些SSR位点的长度进行统计分析可知,白皮松SSR序列长度范围为10 172 bp,其中以长度在10~15 bp的SSR序列数量最多,所占比例最大(2 219,70.13%),其次为长度在16~21 bp的序列(566,17.89%),再次为长度在22~27 bp的序列(160,5.34%)。说明在白皮松转录组中,10~27 bp的短序列(2 954,93.36%)占主导地位。
表4 白皮松转录组SSR位点长度分布特征
Table 4 Distribution characteristics of SSR site length inPinus bungeana transcriptome
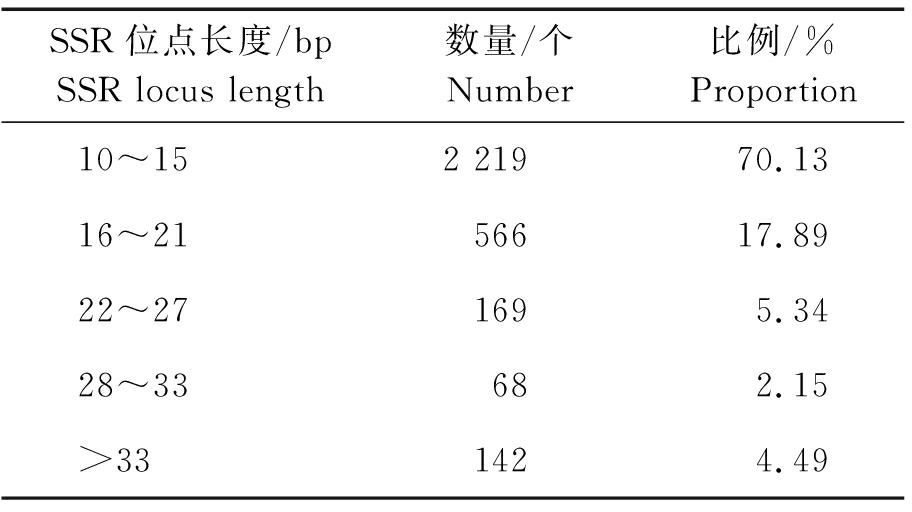
SSR位点长度/bpSSR locus length数量/个Number比例/%Proportion10~152 21970.1316~2156617.8922~271695.3428~33682.15>331424.49
2.2 EST-SSR引物的验证、筛选及多态性分析
对EST-SSR引物的验证、筛选及多态性分析见图1和表5、表6。

图1 26号、53号引物对部分白皮松DNA模板的扩增结果
Figure 1 Amplification of DNA templates of Pinus bungeana by primers 26 and 53
表5 引物基本特征
Table 5 Basic characteristics of primers
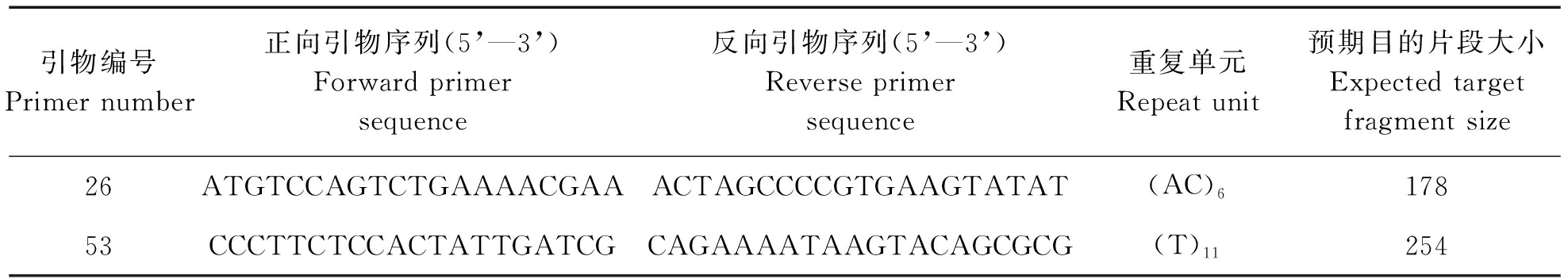
引物编号Primer number正向引物序列(5’—3’)Forward primersequence反向引物序列(5’—3’)Reverse primersequence重复单元Repeat unit预期目的片段大小Expected targetfragment size26ATGTCCAGTCTGAAAACGAAACTAGCCCCGTGAAGTATAT(AC)617853CCCTTCTCCACTATTGATCGCAGAAAATAAGTACAGCGCG(T)11254
表6 不同引物在白皮松中的扩增效果
Table 6 Amplification effect of different primers in Pinus bungeana

引物编号Primer number扩增条带数Number ofamplification bands实际目的片段大小Actual size oftarget fragment多态性条带数Number ofpolymorphic bands多态性信息含量PIC262178 19010.375532254 24510.305
由图1、表5、表6可知,2对多态性的引物共扩增出4个条带,多态性条带2条,引物多态性信息含量分别为0.375和0.305,多态性水平相对较低。
2.3 已发表的白皮松SSR引物的验证分析
表7 已发表的白皮松SSR引物
Table 7 Published SSR primers of Pinus bungeana

引物名称Primer name正向引物序列(5’—3’)Forward primer sequence反向引物序列(5’—3’)Reverse primer sequence36567-992-FCCAGACAACCCAAATGAACAGAATCAGGCGTCCAATRPtest9-FCCAGACAACCCAAATGAAGGGCCTGCTATCGAATCCAGAA919347-FTCGCCTGGGCTTTGTCTGGCGGGTTGCATATTTGGTGssrPt_ctg8767-FTGGGGAAAAATGGCATACATGGAGCAGACACCCATGGACT51113-3237-FTCCAGACAACCCAAATGACAGGCGTCCAATACCAGA48044-7700-FTACGGTGGTCTGTTCTGCAGGCTTCTCCTGGTCTCCPtSIFG_6058RAAGAGGTTGCTCCTCACCAAGCTCCATTTCAGAGCAGGTC
对已发表的白皮松SSR引物的验证分析见图2。
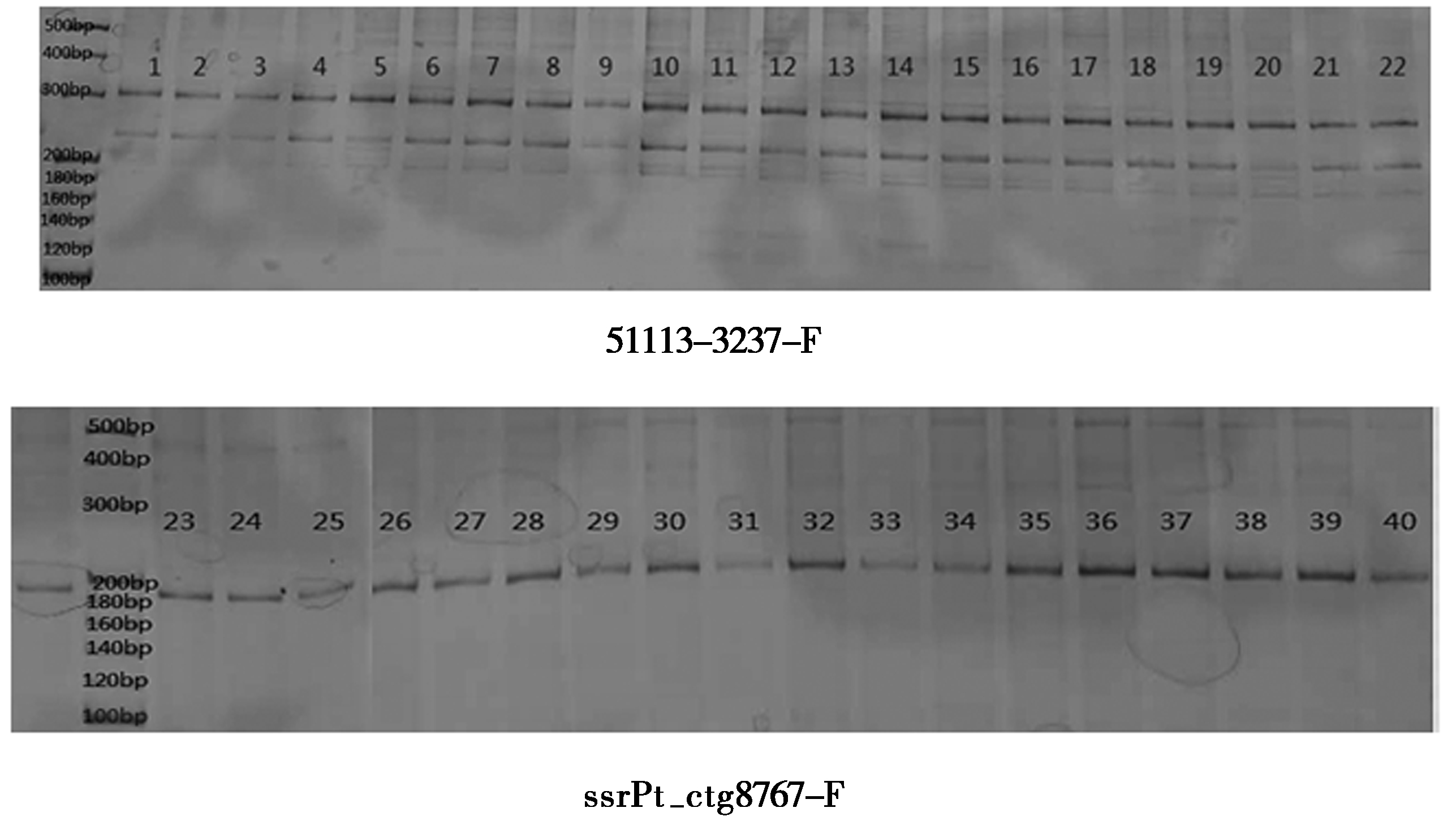
图2 51113-3237-F、ssrPt_ctg8767-F引物对部分白皮松DNA模板的扩增结果
Figure 2 Amplification of DNA templates of Pinus bungeana by primers 51113-3237-F and ssrPt_ctg8767-F
由图2可知,对7对已发表的具有多态性的白皮松引物进行了验证分析,发现其只能扩增出清晰的条带,但对这50株白皮松优树均无多态性,也侧面说明了白皮松基因序列的相对保守性。
3 讨论
随着高通量测序技术以及生物信息学的快速发展,大量的EST数据被注入到NCBI数据库中,极大地提高了引物开发的效率,加速了林木遗传育种研究的发展进程。EST-SSR有很多优点,被广泛应用于品种分类鉴定、种质资源的评价和利用、DNA指纹图谱的构建、遗传多样性检测与分析、分子标记辅助选择育种等方面的研究,但EST-SSR也存在一定的缺点,比如引物有效扩增率偏低、引物多态性较低等,只有通过大量的EST-SSR分子标记开发,才能弥补其缺点[16]。
EST-SSR分子标记开发的目的是为了筛选出扩增条带清晰、多态性高的引物,但在引物的筛选及验证过程中,发现引物的有效扩增率及多态率相对较低,这无疑也加大了引物开发的难度和工作量[16]。本研究中,随机挑选60对EST-SSR引物进行PCR扩增,28对引物能扩增出清晰的条带,其中只有2对引物有多态性,有效扩增率(46.67%)及引物多态率(7.14%)相对较低。在其他物种紫楠(43.62%),牛樟(29.33%),紫斑牡丹(22.73%)等的EST-SSR的引物开发中,同样也发现有效扩增率偏低的问题[17-19]。在其他松科植物的SSR引物开发中,也存在引物多态率较低的问题,如赵罕等人从已发表的309对松属SSR引物中,筛选出了86对白皮松扩增效果较好的引物,其中仅有7对引物有多态性,引物多态率为8.14%[6],而红松和火炬松的引物多态率也仅为15.84%和13.33%[20-21]。究其原因主要有3点:(1)从进化层面来说,松科植物是比较原始的树种,其EST-SSR序列相对保守,变异程度相对较低;(2)所选的植物材料范围相对较窄,样品本身之间的基因差异较小;(3)该物种本身的基因组成及结构也会影响引物的多态性。
由于时间原因,只选择了60对引物进行筛选与验证,开发出的多态性引物较少,在以后的研究中,应该从所设计的引物中再选择更多的引物进行筛选与验证,以期得到更多适用于白皮松的引物,为今后白皮松的研究提供科学的分子依据。
[1] 张开慧,景海斌.白皮松及其遗传多样性研究进展[J].陕西农业科学,2015,61(9):76-78.
[2] 陆素娟,李乡旺.松属的起源、演化及扩散[J].西北林学院学报,1999,14(3):1-5.
[3] 赵罕,郑勇奇,李斌,等.白皮松天然群体遗传多样性的EST-SSR分析[J].林业科学研究, 2014,27(4):474-480.
[4] 李斌,孟庆阳,李言达,等.白皮松种质资源鉴定与评价[J].湖南林业科技,2016,43(2):1-7.
[5] 周惠娟.濒危植物白皮松遗传多样性及遗传结构研究[D].西安:西北大学,2013.
[6] 赵罕.白皮松遗传资源评价及保存策略研究[D].北京:中国林业科学研究院,2012.
[7] 李斌,顾万春,卢宝明.白皮松天然群体种实性状表型多样性研究[J].生物多样性,2002(2):181-188.
[8] XIANG X Y. Genetic diversity and structure of Pinus dabeshanensis revealed by expressed sequence tag-simple sequence repeat(EST-SSR) markers.Biochemical Systematics and Ecology[J].2015,61:70-77.
[9] DUAN D. Comparative Transcriptome Analysis of Male and Female Conelets and Development of Microsatellite Markers in Pinus bungeana,an Endemic Conifer in China[J].Genes,2017,8:393.
[10] YANG Y X. Nucleotide polymorphism and phylogeographic history of an endangered conifer species Pinus bungeana[J].Biochemical Systematics and Ecology,2016,64:89-96.
[11] JIA D M. Survey and analysis of simple sequence repeats (SSRs) in three genomes of Candida species[J].Gene,2016,548(2) :129-135.
[12] GUO Q.Application of simple sequence repeat molecular markers in the study of tree peony[J]. Zhiwu Xuebao (Chinese Bulletin of Botany),2015,50(5):652-664.
[13] QU J B.Genome-wide functional analysis of SSR for an edible mushroom Pleurotus ostreatus[J].Gene,2016, 575(2):524-530.
[14] 周延清.DNA分子标记技术在植物研究中的应用[M].北京:化学工业出版社,2005.
[15] 籍新波.不同海拔天山云杉居群的EST-SSR遗传多样性研究[D].保定:河北农业大学,2012.
[16] 左力辉,张双,梁海永,等.榆树转录组EST-SSR引物开发及遗传多样性分析[J].植物遗传资源学报,2018,19(1):157-166.
[17] 陆云峰,杨安娜,张俊红,等.紫楠转录组EST-SSR标记开发及通用性分析[J].农业生物技术学报,2018,26(6):1014-1024.
[18] 郭莺,孟红岩,林文珍,等.牛樟EST-SSR标记的开发及遗传多态性分析[J].热带作物学报,2018,39(8):1561-1569.
[19] 安宗燕,唐红,李婉茹.基于EST-SSR的紫斑牡丹品种遗传多样性分析[J].分子植物育种,2018,16(20):6744-6752.
[20] 张振,张含国,莫迟,等.红松转录组SSR分析及EST-SSR标记开发[J].林业科学,2015,51(8):114-120.
[21] 张蝶,郭小丹,邓亚婷,等.火炬松SSR-PCR反应体系的建立及引物筛选[J].广西林业科学,2016,45(3):253-258.
[22] 林雪莹.水松EST-SSR分子标记开发及群体遗传变异分析[D].长沙:中南林业科技大学,2018.
[23] 贾婕,冯源恒,杨章旗,等.松属EST-SSR引物开发及马尾松-湿地松种间特异性鉴别引物筛选[J].分子植物育种,2014,12(5):963-968.
[24] 孙海悦,郭瑞雪,徐鉴,等.越橘属植物EST-SSR分子标记开发及遗传多样性分析[J].植物生理学报,2018,54(3):429-440.
[25] 王洪振,王姝,邝盼盼,等.DNA分子标记技术及其在植物育种中的应用[J].吉林师范大学学报:自然科学版,2016,37(1):108-111.
[26] 孙英新,白孝明,王丹丹.蓝莓种质资源遗传多样性的EST-SSR分析[J].辽东学院学报:自然科学版,2018,25(1):31-35.
[27] 李英,胡振亮,胡志霞,等.球孢白僵菌Bb09菌株在美国白蛾僵虫体及其周围土壤中宿存动态[J].林业与生态科学,2018,33(2):172-177.


